Nuove pubblicazioni
Chiarimento dei meccanismi cellulari della parodontite con un modello animale migliorato
Ultima recensione: 14.06.2024

Tutti i contenuti di iLive sono revisionati o verificati da un punto di vista medico per garantire la massima precisione possibile.
Abbiamo linee guida rigorose in materia di sourcing e colleghiamo solo a siti di media affidabili, istituti di ricerca accademici e, ove possibile, studi rivisti dal punto di vista medico. Nota che i numeri tra parentesi ([1], [2], ecc.) Sono link cliccabili per questi studi.
Se ritieni che uno qualsiasi dei nostri contenuti sia impreciso, scaduto o comunque discutibile, selezionalo e premi Ctrl + Invio.
I ricercatori della Tokyo Medical and Dental University (TMDU) hanno sviluppato una tecnica che consente loro di analizzare in dettaglio lo sviluppo della parodontite nel tempo.
La malattia parodontale, rappresentata dalla parodontite, è la principale causa di perdita dei denti e colpisce quasi un adulto su cinque in tutto il mondo. Nella maggior parte dei casi, questa condizione si verifica come risultato di una risposta infiammatoria a un'infezione batterica dei tessuti attorno ai denti.
Quando la condizione peggiora, le gengive iniziano a ritirarsi, esponendo le radici dei denti e l'osso. In particolare, l'incidenza della parodontite aumenta con l'età e, poiché le popolazioni di tutto il mondo aumentano nell'aspettativa di vita, è importante avere una solida comprensione delle sue cause sottostanti e della sua progressione.
In uno studio pubblicato su Nature Communications, i ricercatori della TMDU hanno trovato un modo per raggiungere questo obiettivo migliorando un modello animale ampiamente utilizzato per studiare la parodontite.
Lo studio diretto della parodontite negli esseri umani è difficile. Di conseguenza, gli scienziati si rivolgono spesso a modelli animali per la ricerca preclinica. Ad esempio, il "modello di parodontite indotta da legatura nei topi" ha permesso ai ricercatori, sin dalla sua introduzione nel 2012, di studiare i meccanismi cellulari alla base di questa condizione.
In parole povere, in questo modello la malattia parodontale viene indotta artificialmente posizionando suture di seta sui molari dei topi, il che causa l'accumulo di placca. Sebbene questo metodo sia comodo ed efficace, non copre il quadro completo della parodontite.
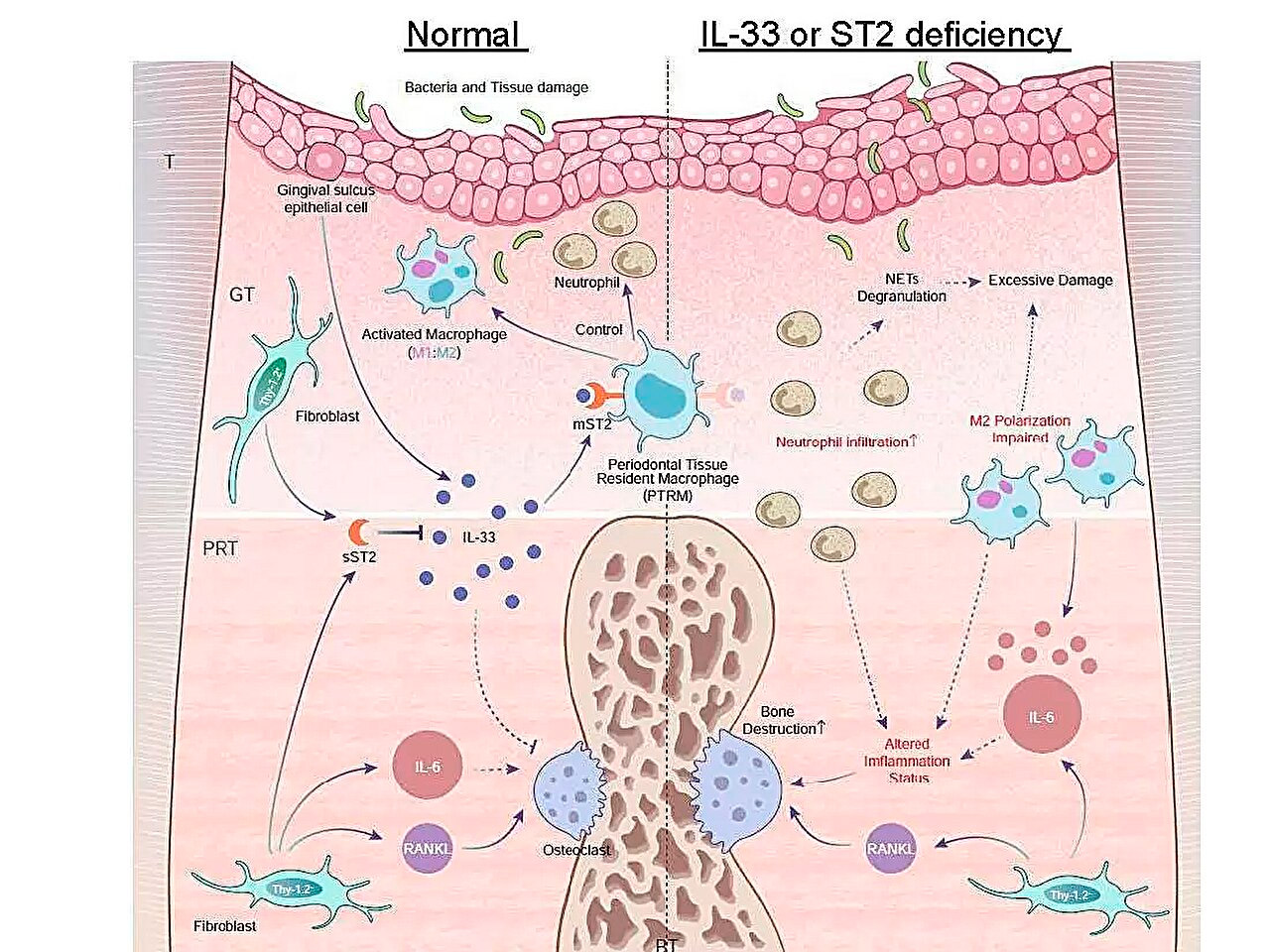
Illustrazione schematica dei profili di espressione genica infiammatoria durante la parodontite e il ruolo dell'asse IL-33/ST2 nel controllo dell'infiammazione acuta. Fonte: Tokyo Medical and Dental University.
"Sebbene il tessuto parodontale sia composto da gengiva, legamento parodontale, osso alveolare e cemento, l'analisi viene solitamente eseguita esclusivamente su campioni gengivali a causa di limitazioni tecniche e quantitative", osserva l'autore principale dello studio Anhao Liu. "Questa strategia di campionamento limita le conclusioni che si possono trarre da questi studi, quindi sono necessari metodi in grado di analizzare tutti i componenti dei tessuti simultaneamente".
Per affrontare questa limitazione, il team di ricerca ha sviluppato un modello modificato di parodontite indotta da legatura. Invece della classica legatura singola, hanno utilizzato una legatura tripla sul molare superiore sinistro dei topi maschi. Questa strategia ha ampliato l'area di perdita ossea senza significativa distruzione ossea attorno al secondo molare, aumentando il numero di diversi tipi di tessuto parodontale.
"Abbiamo isolato tre tipi di tessuto principali e valutato la resa di RNA tra i due modelli. I risultati hanno mostrato che il modello a tripla legatura ha effettivamente aumentato la resa, ottenendo quattro volte la quantità di tessuto periradicolare normale e supportando l'analisi ad alta risoluzione di diversi tipi di tessuto," spiega Sr. Del Dr. Mikihito Hayashi.
Dopo aver confermato l'efficacia del loro modello modificato, i ricercatori hanno iniziato a studiare gli effetti della parodontite sull'espressione genetica tra diversi tipi di tessuto nel tempo, concentrandosi sui geni associati all'infiammazione e alla differenziazione degli osteoclasti.
Uno dei risultati principali è stato che l'espressione del gene Il1rl1 era significativamente più alta nel tessuto periradicolare cinque giorni dopo la legatura. Questo gene codifica per la proteina ST2 nelle isoforme del recettore e dell'esca, che si lega a una citochina chiamata IL-33, che è coinvolta nei processi infiammatori e immunoregolatori.
Per ottenere ulteriori informazioni sul ruolo di questo gene, il team ha indotto la parodontite in topi geneticamente modificati privi dei geni Il1rl1 o Il33. Questi topi hanno dimostrato una distruzione ossea infiammatoria accelerata, evidenziando il ruolo protettivo della via IL-33/ST2. Ulteriori analisi delle cellule contenenti la proteina ST2 nella sua forma recettoriale, mST2, hanno mostrato che la maggior parte derivava da macrofagi.
"I macrofagi sono generalmente classificati in due tipi principali, proinfiammatori e antinfiammatori, a seconda della loro attivazione. Abbiamo scoperto che le cellule che esprimono mST2 sono uniche in quanto esprimono contemporaneamente alcuni marcatori di entrambi i tipi di macrofagi," commenta autore senior Dr. Takanori Iwata. "Queste cellule erano presenti nel tessuto periradicolare prima dell'inizio dell'infiammazione, per questo le abbiamo chiamate 'macrofagi parodontali residenti.'"
Nel loro insieme, i risultati di questo studio dimostrano il potere del modello animale modificato di studiare la parodontite su una scala più dettagliata, fino al livello biomolecolare.
"Proponiamo la possibilità di un nuovo percorso molecolare, IL-33/ST2, che regola l'infiammazione e la distruzione ossea nella malattia parodontale, insieme a macrofagi specifici nel tessuto periradicolare, che è profondamente coinvolto nella malattia parodontale. Si spera che questo porti allo sviluppo di nuove strategie di trattamento e metodi di prevenzione", conclude l'autore senior, il dottor Tomoki Nakashima.
