Nuove pubblicazioni
Identificata la proteina responsabile di una malattia infiammatoria genetica
Ultima recensione: 02.07.2025

Tutti i contenuti di iLive sono revisionati o verificati da un punto di vista medico per garantire la massima precisione possibile.
Abbiamo linee guida rigorose in materia di sourcing e colleghiamo solo a siti di media affidabili, istituti di ricerca accademici e, ove possibile, studi rivisti dal punto di vista medico. Nota che i numeri tra parentesi ([1], [2], ecc.) Sono link cliccabili per questi studi.
Se ritieni che uno qualsiasi dei nostri contenuti sia impreciso, scaduto o comunque discutibile, selezionalo e premi Ctrl + Invio.
Un team di ricercatori guidato dal Dott. Hirotsugu Oda del Cluster of Excellence for Aging Research del CECAD presso l'Università di Colonia ha scoperto il ruolo di un determinato complesso proteico in alcune forme di disregolazione immunitaria. Questo risultato potrebbe portare allo sviluppo di nuovi approcci terapeutici volti a ridurre l'autoinsufficienza e a "ripristinare" il sistema immunitario dei pazienti affetti da una disfunzione genetica di questo complesso proteico.
Lo studio, intitolato "La perdita di funzione della proteina SHARPIN umana biallelica induce autoinfiammazione e immunodeficienza", è stato pubblicato sulla rivista Nature Immunology.
Il complesso lineare di assemblaggio dell'ubiquitina (LUBAC), composto dalle proteine HOIP, HOIL-1 e SHARPIN, è da tempo riconosciuto per il suo ruolo cruciale nel mantenimento dell'omeostasi immunitaria. Precedenti studi sui topi hanno dimostrato le gravi conseguenze della perdita di SHARPIN, che porta a gravi dermatiti dovute all'eccessiva morte delle cellule cutanee. Tuttavia, le specifiche conseguenze sulla salute della carenza di SHARPIN negli esseri umani sono rimaste poco chiare.
Il team di ricerca ha segnalato per la prima volta due persone con deficit di SHARPIN che manifestavano sintomi di autoinflazione e immunodeficienza, ma inaspettatamente non mostravano problemi dermatologici come nei topi.
Ulteriori indagini hanno evidenziato che questi individui presentavano una risposta canonica compromessa di NF-κB, un importante pathway di risposta immunitaria. Presentavano inoltre una maggiore suscettibilità alla morte cellulare indotta da membri della superfamiglia del fattore di necrosi tumorale (TNF). Il trattamento di un paziente con deficit di SHARPIN con una terapia anti-TNF, che inibisce specificamente la morte cellulare indotta da TNF, ha portato alla completa risoluzione dell'autoinsufflazione a livello cellulare e alla presentazione clinica.
Lo studio dimostra che la morte cellulare eccessiva e incontrollata gioca un ruolo cruciale nelle malattie infiammatorie genetiche umane. Il team di Oda ha aggiunto la carenza di SHARPIN a un gruppo di malattie infiammatorie genetiche umane che propone di chiamare "errori congeniti della morte cellulare".
Protezione contro la disregolazione immunitaria Lo studio è stato avviato nel laboratorio del Dr. Dan Kastner presso i National Institutes of Health (NIH) negli Stati Uniti. Gli scienziati hanno avuto l'opportunità di osservare un paziente con episodi inspiegabili di febbre, artrite, colite e immunodeficienza, manifestatisi durante l'infanzia.
Dopo aver ottenuto il consenso informato, hanno eseguito il sequenziamento dell'esoma sul paziente e sui suoi familiari, scoprendo che il paziente presentava una variante genetica devastante nel gene SHARPIN, che portava a livelli non rilevabili della proteina SHARPIN. Hanno inoltre scoperto che le cellule del paziente mostravano una maggiore propensione a morire, sia nelle cellule in coltura che nelle biopsie del paziente.
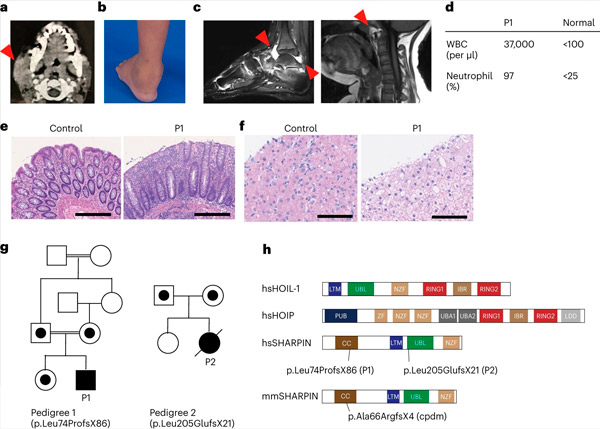
La carenza di SHARPIN negli esseri umani causa autoinfiammazione e glicogenosi epatica. Fonte: Nature Immunology (2024). DOI: 10.1038/s41590-024-01817-w
Il team ha anche scoperto che lo sviluppo dei centri germinali linfoidi – microstrutture specializzate nelle adenoidi fondamentali per la maturazione dei linfociti B del nostro sistema immunitario e, di conseguenza, per la produzione di anticorpi – era significativamente ridotto a causa dell'aumentata morte dei linfociti B. Questi risultati spiegano l'immunodeficienza dei pazienti e sottolineano l'importante ruolo del LUBAC nel mantenimento dell'omeostasi immunitaria negli esseri umani.
"Il nostro studio evidenzia l'importanza cruciale di LUBAC nella protezione dalla disregolazione immunitaria. Chiarire i meccanismi molecolari alla base della carenza di LUBAC, apre la strada a nuove strategie terapeutiche volte a ripristinare l'omeostasi immunitaria", ha affermato Oda, autore principale dello studio.
Ha aggiunto: "Uno dei pazienti con deficit di SHARPIN era costretto su una sedia a rotelle da anni prima che lo visitassimo per la prima volta. Le sue caviglie erano infiammate e camminare era troppo doloroso. La diagnosi genetica ci ha permesso di individuare il percorso molecolare corretto alla base delle sue condizioni."
Da quando il paziente ha iniziato la terapia anti-TNF, è asintomatico da quasi sette anni. "Come medico e scienziato, sono lieto di avere l'opportunità di avere un impatto positivo sulla vita di un paziente attraverso la nostra ricerca", ha concluso Oda.
