Nuove pubblicazioni
Nuovi meccanismi genetici potrebbero essere un bersaglio terapeutico contro il glioma
Ultima recensione: 02.07.2025

Tutti i contenuti di iLive sono revisionati o verificati da un punto di vista medico per garantire la massima precisione possibile.
Abbiamo linee guida rigorose in materia di sourcing e colleghiamo solo a siti di media affidabili, istituti di ricerca accademici e, ove possibile, studi rivisti dal punto di vista medico. Nota che i numeri tra parentesi ([1], [2], ecc.) Sono link cliccabili per questi studi.
Se ritieni che uno qualsiasi dei nostri contenuti sia impreciso, scaduto o comunque discutibile, selezionalo e premi Ctrl + Invio.
Uno studio condotto dal laboratorio di Shi-Yuan Cheng, PhD, professore presso la Divisione di Neuro-Oncologia Ken and Ruth Davey del Dipartimento di Neurologia, ha identificato nuovi meccanismi alla base degli eventi di splicing alternativo dell'RNA nelle cellule tumorali del glioma, che potrebbero fungere da nuovi bersagli terapeutici. I risultati dello studio sono pubblicati sul Journal of Clinical Investigation.
"Abbiamo trovato un modo diverso per trattare il glioma attraverso la lente dello splicing alternativo e scoperto nuovi bersagli che non erano stati identificati in precedenza ma che sono importanti per la malignità del glioma", ha affermato Xiao Song, MD, PhD, professore associato di neurologia e autore principale dello studio.
I gliomi sono il tipo più comune di tumore cerebrale primario negli adulti e hanno origine dalle cellule gliali, che risiedono nel sistema nervoso centrale e supportano i neuroni adiacenti. I gliomi sono altamente resistenti ai trattamenti standard, tra cui radioterapia e chemioterapia, a causa dell'eterogeneità genetica ed epigenetica del tumore, evidenziando la necessità di trovare nuovi bersagli terapeutici.
Una precedente ricerca del laboratorio di Cheng, pubblicata sulla rivista Cancer Research, ha dimostrato che l'importante fattore di splicing SRSF3 è significativamente elevato nei gliomi rispetto al cervello normale e che lo splicing dell'RNA regolato da SRSF3 promuove la crescita e la progressione del glioma influenzando molteplici processi cellulari nelle cellule tumorali.
Lo splicing dell'RNA è un processo che comporta la rimozione degli introni (regioni non codificanti dell'RNA) e l'unione degli esoni (regioni codificanti) per formare una molecola di mRNA matura che supporta l'espressione genica in una cellula.
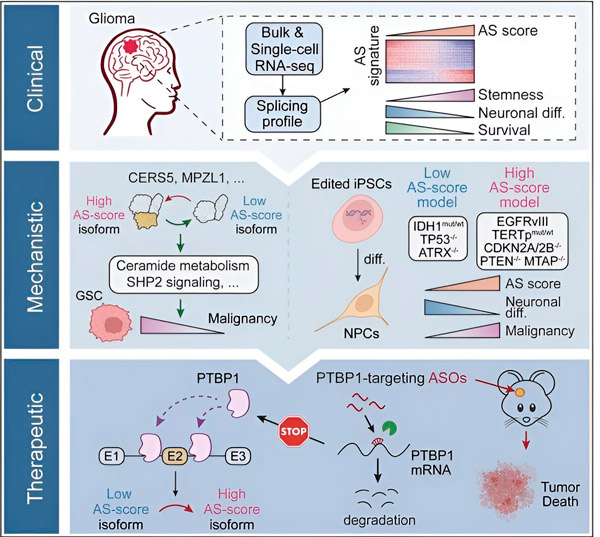
Nel presente studio, gli scienziati si sono prefissati di identificare le alterazioni nello splicing alternativo nelle cellule tumorali del glioma, i meccanismi alla base di tali alterazioni e di determinare il loro potenziale come bersagli terapeutici.
Utilizzando metodi computazionali e tecnologie di sequenziamento dell'RNA, i ricercatori hanno esaminato i cambiamenti di splicing nelle cellule tumorali di glioma da campioni di pazienti. Per confermare questi cambiamenti, hanno utilizzato tecnologie di editing genetico CRISPR per introdurre diverse mutazioni driver del glioma in modelli di glioma derivati da cellule staminali pluripotenti indotte umane (iPSC).
Hanno scoperto che queste alterazioni dello splicing sono potenziate da una variante del recettore del fattore di crescita epidermico III (EGFRIII), che è noto per essere sovraespresso in molti tumori, compresi i gliomi, e sono inibite da una mutazione nel gene IDH1.
I ricercatori hanno confermato la funzione di due eventi di splicing dell'RNA che creano diverse isoforme proteiche con diverse sequenze di amminoacidi.
"Solo una di queste isoforme può promuovere la crescita tumorale, a differenza dell'altra isoforma, che è normalmente espressa nel cervello normale. I tumori sfruttano questo meccanismo per esprimere selettivamente l'isoforma che promuove la crescita tumorale rispetto all'isoforma cerebrale normale", ha affermato Song.
Il team ha poi analizzato le proteine a monte che legano l'RNA e ha scoperto che il gene PTBP1 regola lo splicing dell'RNA che promuove il tumore nelle cellule di glioma. Utilizzando un modello di glioma ortotopico in topi immunodeficienti, i ricercatori hanno mirato a PTBP1 con una terapia a base di oligonucleotidi antisenso (ASO), che alla fine ha soppresso la crescita tumorale.
"I nostri dati evidenziano il ruolo dello splicing alternativo dell'RNA nell'influenzare la malignità e l'eterogeneità del glioma e il suo potenziale come vulnerabilità terapeutica per il trattamento dei gliomi adulti", hanno scritto gli autori dello studio.
Il prossimo passo per i ricercatori sarà esplorare la possibilità di colpire PTBP1 per suscitare una risposta immunitaria antitumorale, ha affermato Song.
"Utilizzando l'analisi di sequenziamento dell'RNA a lettura lunga, abbiamo scoperto che il targeting di PTBP1 nelle cellule di glioma porta alla produzione di molteplici trascritti con splicing alternativo, assenti nei tessuti normali. Il nostro prossimo progetto è quindi scoprire se questa isoforma possa generare alcuni antigeni in modo che il sistema immunitario possa riconoscere meglio il tumore", ha affermato Song.
Song ha anche aggiunto che il suo team è interessato ad analizzare i cambiamenti di splicing nelle cellule non tumorali dei pazienti affetti da glioma, come le cellule immunitarie.
Sappiamo già che lo splicing è molto importante per la regolazione della funzione cellulare, quindi non dovrebbe solo regolare la malignità tumorale, ma può anche regolare la funzione delle cellule immunitarie per determinare se siano in grado di uccidere efficacemente il cancro. Stiamo quindi conducendo analisi bioinformatiche su cellule immunitarie infiltrate dal tumore per verificare se si verifichi un cambiamento nello splicing dopo che una cellula immunitaria si è infiltrata nel tumore.
"Il nostro obiettivo è determinare il ruolo dello splicing alternativo nel modellare il microambiente tumorale immunosoppressivo e identificare potenziali bersagli per migliorare l'efficacia delle immunoterapie nel glioma", ha affermato Song.
