Nuove pubblicazioni
Un sistema di somministrazione di farmaci a circuito chiuso potrebbe migliorare la somministrazione della chemioterapia
Ultima recensione: 02.07.2025

Tutti i contenuti di iLive sono revisionati o verificati da un punto di vista medico per garantire la massima precisione possibile.
Abbiamo linee guida rigorose in materia di sourcing e colleghiamo solo a siti di media affidabili, istituti di ricerca accademici e, ove possibile, studi rivisti dal punto di vista medico. Nota che i numeri tra parentesi ([1], [2], ecc.) Sono link cliccabili per questi studi.
Se ritieni che uno qualsiasi dei nostri contenuti sia impreciso, scaduto o comunque discutibile, selezionalo e premi Ctrl + Invio.
Quando i pazienti oncologici si sottopongono a chemioterapia, le dosi della maggior parte dei farmaci vengono calcolate in base alla superficie corporea del paziente. Questa viene stimata utilizzando un'equazione che tiene conto dell'altezza e del peso del paziente. Questa equazione è stata formulata nel 1916 sulla base dei dati di soli nove pazienti.
Questo approccio semplificato al dosaggio non tiene conto di altri fattori e può comportare la somministrazione di una dose eccessiva o insufficiente di farmaco al paziente. Di conseguenza, alcuni pazienti potrebbero manifestare una tossicità non necessaria o un'efficacia insufficiente della chemioterapia somministrata.
Per migliorare l'accuratezza del dosaggio della chemioterapia, gli ingegneri del MIT hanno sviluppato un approccio alternativo che consente di personalizzare la dose per ciascun paziente. Il loro sistema misura la quantità di farmaco presente nell'organismo del paziente e invia tali dati a un controller in grado di regolare di conseguenza la velocità di infusione.
Questo approccio potrebbe aiutare a compensare le differenze nella farmacocinetica dei farmaci causate dalla composizione corporea, dalla predisposizione genetica, dalla tossicità d'organo indotta dalla chemioterapia, dalle interazioni con altri farmaci e alimenti e dalle variazioni circadiane negli enzimi responsabili della scomposizione dei farmaci chemioterapici, affermano i ricercatori.
"Riconoscendo i progressi nella comprensione del modo in cui i farmaci vengono metabolizzati e applicando strumenti ingegneristici per semplificare il dosaggio personalizzato, crediamo di poter contribuire a trasformare la sicurezza e l'efficacia di molti farmaci", ha affermato Giovanni Traverso, professore associato di ingegneria meccanica al MIT, gastroenterologo al Brigham and Women's Hospital e autore principale dello studio.
Louis DeRidder, studente laureato al MIT, è l'autore principale dell'articolo pubblicato sulla rivista Med.
Monitoraggio continuo
In questo studio, i ricercatori si sono concentrati su un farmaco chiamato 5-fluorouracile, utilizzato per il trattamento del cancro del colon-retto e di altri tumori. Il farmaco viene in genere somministrato nell'arco di 46 ore e il suo dosaggio viene determinato utilizzando una formula basata sull'altezza e sul peso del paziente, che fornisce una stima della superficie corporea.
Tuttavia, questo approccio non tiene conto delle differenze nella composizione corporea che possono influenzare la distribuzione del farmaco nell'organismo, né delle variazioni genetiche che ne influenzano il metabolismo. Queste differenze possono portare a effetti collaterali dannosi in caso di somministrazione di una dose eccessiva di farmaco. Se la dose non è sufficiente, il tumore potrebbe non essere eliminato come previsto.
"Le persone con la stessa superficie corporea possono avere altezze e pesi molto diversi, una massa muscolare diversa o una genetica diversa, ma finché altezza e peso inseriti in questa equazione producono la stessa superficie corporea, la loro dose è identica", afferma DeRidder, dottorando nel programma di ingegneria medica e fisica medica presso l'Harvard-MIT Program in Health Sciences and Technology.
Un altro fattore che può alterare la quantità di farmaco nel sangue in un dato momento è la variazione circadiana di un enzima chiamato diidropirimidina deidrogenasi (DPD), che scompone il 5-fluorouracile. L'espressione della DPD, come quella di molti altri enzimi nell'organismo, è regolata da un ritmo circadiano. Pertanto, la degradazione del 5-FU da parte della DPD non è costante, ma varia con l'ora del giorno. Questi ritmi circadiani possono determinare una variazione di dieci volte superiore nella quantità di 5-FU nel sangue di un paziente durante un'infusione.
"Utilizzando la superficie corporea per calcolare la dose di chemioterapia, sappiamo che due persone possono avere tossicità molto diverse dal 5-fluorouracile. Un paziente può sottoporsi a cicli di trattamento con tossicità minima e poi a un ciclo con tossicità elevata. Qualcosa è cambiato nel modo in cui il paziente ha metabolizzato la chemioterapia da un ciclo all'altro. Il nostro obsoleto metodo di dosaggio non tiene conto di questi cambiamenti e i pazienti ne soffrono", afferma Douglas Rubinson, oncologo clinico presso il Dana-Farber Cancer Institute e autore dello studio.
Un modo per cercare di compensare la variabilità nella farmacocinetica della chemioterapia è una strategia chiamata monitoraggio terapeutico del farmaco, in cui il paziente fornisce un campione di sangue al termine di un ciclo di trattamento. Dopo che questo campione è stato analizzato per le concentrazioni del farmaco, il dosaggio può essere aggiustato, se necessario, all'inizio del ciclo successivo (di solito due settimane per il 5-fluorouracile).
È stato dimostrato che questo approccio porta a risultati migliori per i pazienti, ma non è stato ampiamente utilizzato per chemioterapie come quella a base di 5-fluorouracile.
I ricercatori del MIT volevano sviluppare un tipo di monitoraggio simile, ma in modo automatizzato, che consentisse di personalizzare il dosaggio dei farmaci in tempo reale, il che avrebbe potuto portare a risultati migliori per i pazienti.
Nel loro sistema a circuito chiuso, le concentrazioni del farmaco possono essere monitorate costantemente e queste informazioni vengono utilizzate per regolare automaticamente la velocità di infusione del farmaco chemioterapico, in modo da mantenere la dose entro l'intervallo target.
Questo sistema a circuito chiuso consente di personalizzare il dosaggio del farmaco tenendo conto dei ritmi circadiani dei livelli degli enzimi che metabolizzano il farmaco, nonché di eventuali cambiamenti nella farmacocinetica del paziente dall'ultimo trattamento, come la tossicità d'organo indotta dalla chemioterapia.
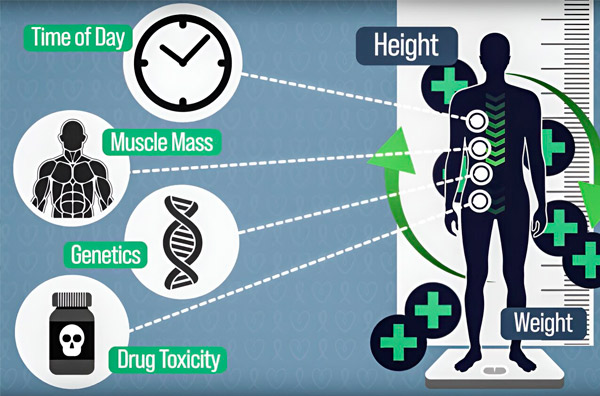
Per rendere il dosaggio della chemioterapia più preciso, gli ingegneri del MIT hanno sviluppato un metodo per misurare costantemente la quantità di farmaco presente nel corpo di un paziente durante un'infusione di diverse ore. Questo aiuterà a compensare le differenze causate dalla composizione corporea, dalla genetica, dalla tossicità del farmaco e dalle oscillazioni circadiane. Fonte: Per gentile concessione dei ricercatori.
Il nuovo sistema sviluppato dai ricercatori, denominato CLAUDIA (Closed-Loop AUtomated Drug Infusion RegulAtor), utilizza apparecchiature disponibili in commercio per ogni fase. I campioni di sangue vengono prelevati ogni cinque minuti e preparati rapidamente per l'analisi. La concentrazione di 5-fluorouracile nel sangue viene misurata e confrontata con l'intervallo target.
La differenza tra la concentrazione target e quella misurata viene inserita in un algoritmo di controllo, che poi regola la velocità di infusione secondo necessità per mantenere la dose entro l'intervallo di concentrazioni in cui il farmaco è efficace e non tossico.
"Abbiamo sviluppato un sistema che ci consente di misurare costantemente la concentrazione del farmaco e di regolare di conseguenza la velocità di infusione per mantenere la concentrazione del farmaco nella finestra terapeutica", afferma DeRidder.
Regolazione rapida
Nei test sugli animali, i ricercatori hanno scoperto che utilizzando CLAUDIA riuscivano a mantenere la quantità di farmaco in circolazione nell'organismo entro l'intervallo target per circa il 45 percento del tempo.
I livelli di farmaco negli animali sottoposti a chemioterapia senza CLAUDIA sono rimasti, in media, nell'intervallo target solo nel 13% dei casi. I ricercatori non hanno testato l'efficacia dei livelli di farmaco in questo studio, ma si ritiene che il mantenimento delle concentrazioni nella finestra target si traduca in risultati migliori e minore tossicità.
CLAUDIA è stata inoltre in grado di mantenere la dose di 5-fluorouracile nell'intervallo target anche quando è stato somministrato un farmaco che inibisce l'enzima DPD. Negli animali trattati con questo inibitore senza monitoraggio e aggiustamento continui, i livelli di 5-fluorouracile sono aumentati fino a otto volte.
Per questa dimostrazione, i ricercatori hanno eseguito manualmente ogni fase del processo utilizzando apparecchiature disponibili in commercio, ma ora intendono automatizzare ogni passaggio in modo che il monitoraggio e gli aggiustamenti della dose possano essere effettuati senza l'intervento umano.
Per misurare le concentrazioni del farmaco, i ricercatori hanno utilizzato la cromatografia liquida ad alte prestazioni con spettrometria di massa (HPLC-MS), una tecnica che può essere adattata per rilevare quasi tutti i tipi di farmaco.
"Prevediamo un futuro in cui potremo utilizzare CLAUDIA per qualsiasi farmaco che abbia le appropriate proprietà farmacocinetiche e sia rilevabile tramite HPLC-MS, consentendo un dosaggio personalizzato per molti farmaci diversi", afferma DeRidder.
