Nuove pubblicazioni
Neuroprotesi per il tratto gastrointestinale: ripristina la peristalsi e attiva gli "ormoni della sazietà"
Ultima recensione: 18.08.2025

Tutti i contenuti di iLive sono revisionati o verificati da un punto di vista medico per garantire la massima precisione possibile.
Abbiamo linee guida rigorose in materia di sourcing e colleghiamo solo a siti di media affidabili, istituti di ricerca accademici e, ove possibile, studi rivisti dal punto di vista medico. Nota che i numeri tra parentesi ([1], [2], ecc.) Sono link cliccabili per questi studi.
Se ritieni che uno qualsiasi dei nostri contenuti sia impreciso, scaduto o comunque discutibile, selezionalo e premi Ctrl + Invio.
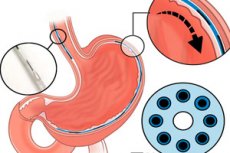
I disturbi della motilità gastrointestinale (esofago e stomaco) – acalasia, gastroparesi, disfagia, ecc. – colpiscono oltre il 20% della popolazione e causano morbilità e costi significativi. Gli approcci standard – farmaci, interventi comportamentali e chirurgia – hanno spesso un'efficacia limitata e non ripristinano la peristalsi coordinata.
- Perché i dispositivi esistenti non risolvono il problema. La stimolazione elettrica del tratto gastrointestinale è stata studiata fin dagli anni '60, ma gli impianti clinicamente approvati (ad esempio, Enterra per la gastroparesi, gli stimolatori vagali VBLOC per l'obesità, la stimolazione sacrale InterStim per l'incontinenza fecale) operano principalmente a circuito aperto e spesso producono effetti incoerenti sullo svuotamento gastrico. Il motivo è che una o più sorgenti di corrente con parametri costanti non riproducono la complessità spaziotemporale della peristalsi naturale.
- Fisiologia che deve essere "imitata". La peristalsi è un circuito chiuso: segnali sensoriali (stiramento, temperatura, stimoli chimici) → risposte riflesse nel plesso mienterico e nella muscolatura liscia. Oltre al trasporto del cibo, la motilità influenza i segnali afferenti intestino-cervello e gli ormoni della sazietà (GLP-1, insulina, grelina), determinando l'appetito e il senso di sazietà. In caso di dismotilità, questi circuiti sono interrotti.
- Lacuna tecnologica. Per riprodurre le onde "corrette", è necessaria una stimolazione multicanale direttamente in prossimità del plesso mienterico e dello strato muscolare. Tuttavia, l'accesso a queste zone richiede solitamente un intervento chirurgico invasivo; le tecniche endoscopiche avanzate (ad esempio, NOTES) sono complesse e non ampiamente utilizzate. Sono necessari strumenti mininvasivi che consentano il posizionamento preciso degli elettrodi nella sottomucosa e funzionino in un circuito chiuso "sensing → stimolazione".
- Cosa offre il nuovo lavoro. Gli autori descrivono una neuroprotesi multicanale installata per via endoscopica con stimolazione elettrica e chimica, in grado di innescare onde peristaltiche coordinate in risposta a un segnale relativo al passaggio di un bolo, non solo ripristinando la motilità, ma anche modulando la risposta metabolica (avvicinandola a uno stato di "nutrimento"). Questo colma lacune chiave: accesso allo strato desiderato, coordinazione spaziotemporale e funzionamento a circuito chiuso.
In breve: esiste una nicchia clinica ampia: dismotivazioni diffuse e scarsamente trattate. I precedenti stimolanti "aperti" non imitano la fisiologia naturale. Pertanto, è logico cercare di insegnare all'impianto a "pensare come il tratto gastrointestinale": percepire il bolo e innescare la peristalsi fisiologica esattamente dove passa il segnale naturale: a livello del plesso mioenterico.
Un team del MIT, di Harvard e di Brigham and Women's ha creato un impianto esofageo/stomaco in miniatura che rileva un bolo alimentare in un "circuito chiuso" e innesca onde coordinate di peristalsi. Nei suini, il dispositivo non solo ha ripristinato la motilità esofagea e gastrica, ma ha anche indotto cambiamenti ormonali simili a quelli dello stato postprandiale (dopo mangiato). L'impianto viene posizionato per via endoscopica, senza intervento chirurgico addominale. Lo studio è stato pubblicato sulla rivista Nature.
Cosa hanno inventato?
- L'impianto stesso. Una sottile neuroprotesi "fibrosa" con un diametro di circa 1,25 mm, dotata di sette elettrodi ogni 1 cm e di un microcanale per la somministrazione locale di sostanze (elettrostimolazione e chemistimolazione). La sua flessibilità e le sue dimensioni ne consentono l'inserimento attraverso il canale strumentale standard di un endoscopio (2,8-3,2 mm).
- Installazione. È stato sviluppato uno strumento endoscopico: un ago con un "uncino" in nitinol a trazione inversa, idrodissezione e il trucco chiave: la ricerca della sottomucosa tramite impedenza tissutale per un posizionamento preciso appena sopra lo strato muscolare, vicino al plesso mienterico.
- Circuito chiuso. Il sistema legge il segnale del bolo (EMG/sensori intraluminali) e seleziona un pattern di stimolazione per indurre contrazioni sequenziali simili alla peristalsi naturale. È possibile combinare stimoli "eccitatori" e "inibitori", nonché rilassare localmente gli sfinteri con microdosi di farmaci.
Cosa è stato mostrato sugli animali
- Esofago: l'impianto ha prodotto "onde di deglutizione" senza deglutizione effettiva, tra cui il rilassamento controllato dello sfintere esofageo inferiore (tramite micro-somministrazione di glucagone) e onde avanti/retrograde programmabili, in pratica un "joystick" peristaltico.
- Stomaco. Dopo 20 minuti di stimolazione, la frequenza della peristalsi è aumentata di circa due volte rispetto al controllo (n≈4, p<0,05).
- "Illusione di sazietà" metabolica. In condizioni di digiuno, la stimolazione di 30 minuti (esofago o stomaco) ha portato a cambiamenti ormonali: un aumento di GLP-1 e insulina, una diminuzione della grelina (ormone dell'appetito); con la stimolazione gastrica, è stato osservato anche un aumento del glucagone. Il profilo nel complesso assomigliava allo stato postprandiale.
Dettagli di sicurezza e ingegneria
Brevi test di biocompatibilità in vitro (estratti di materiale) non hanno evidenziato alcuna tossicità; in vivo, 7 giorni dopo l'impianto, normale estensibilità della parete e nessuna migrazione del dispositivo/danno tissutale macroscopico. (Ulteriori test di durabilità e affidabilità richiedono test a lungo termine.)
Perché è necessario?
- Disturbi della motilità e condizioni refrattarie. Acalasia, gastroparesi, disfagia, disturbi postoperatori, dove i farmaci/interventi chirurgici classici spesso hanno un effetto incompleto. La stimolazione multicanale locale è più vicina alla fisiologia reale rispetto agli attuali impianti a circuito aperto "monocanale".
- Disturbi metabolici. Controllando le vie afferenti intestino-cervello, il dispositivo potrebbe potenzialmente modulare l'appetito e il metabolismo, il che è interessante per l'obesità/diabete (ipotesi finora, nessuna prova nell'uomo).
Limitazioni e cosa succederà dopo
Si tratta di un lavoro preclinico sui suini, in fase acuta-subacuta. Ci attendono studi a lungo termine sulla stabilità del contatto, l'apporto energetico, il rischio di fibrosi, protocolli di stimolazione precisi e poi i primi studi clinici su pazienti con gravi forme di dismotività. Ma è già stato dimostrato che la peristalsi può essere "attivata" a comando e che le risposte ormonali possono essere indirizzate verso la sazietà, il tutto attraverso l'accesso endoscopico.
