Esperto medico dell'articolo
Nuove pubblicazioni
Farmaci
Halidor
Ultima recensione: 03.07.2025

Tutti i contenuti di iLive sono revisionati o verificati da un punto di vista medico per garantire la massima precisione possibile.
Abbiamo linee guida rigorose in materia di sourcing e colleghiamo solo a siti di media affidabili, istituti di ricerca accademici e, ove possibile, studi rivisti dal punto di vista medico. Nota che i numeri tra parentesi ([1], [2], ecc.) Sono link cliccabili per questi studi.
Se ritieni che uno qualsiasi dei nostri contenuti sia impreciso, scaduto o comunque discutibile, selezionalo e premi Ctrl + Invio.
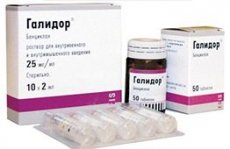
Il farmaco Galidor (sinonimi: Bencyclane, Bencyclane fumarate, Bencyclamide, Angiocyclane) appartiene al gruppo farmacologico degli antispastici miotropici, che, riducendo il tono muscolare dei tessuti degli organi interni e dei vasi sanguigni, alleviano gli spasmi.
 [ 1 ]
[ 1 ]
Indicazioni Galidora
Il farmaco Halidor è utilizzato nella terapia complessa delle patologie dei vasi sanguigni associate al loro restringimento (stenosi) o al blocco completo (occlusione). Tra queste, l'aterosclerosi obliterante, l'endoarterite obliterante (tromboangioite) e le forme periferiche di aortoarterite aspecifica. Halidor è utilizzato anche per le patologie dei vasi oculari (ostruzione dell'arteria retinica centrale, angiopatia diabetica, ecc.).
Il farmaco è prescritto nelle patologie dei vasi cerebrali (forme acute e croniche di ischemia cerebrale), negli spasmi dei vasi periferici caratteristici dell'acrocinosi, della sindrome di Raynaud idiopatica e del pernio.
Le indicazioni per l'uso di Galidor sono le malattie del tratto gastrointestinale e dell'apparato urinario accompagnate da spasmi degli organi interni: gastroenterite, ulcera gastrica e duodenale, colecistite, colelitiasi, colite, discinesia spastica del colon, frequente stimolo doloroso a defecare (tenesmo), flatulenza dopo interventi chirurgici, spasmi e tenesmo della vescica.
Modulo per il rilascio
Il farmaco Galidor è disponibile in due forme: compresse (100 mg) e soluzione al 2,5% (in fiale da 2 ml) per iniezioni endovenose e intramuscolari.
 [ 2 ]
[ 2 ]
Farmacodinamica
L'effetto terapeutico del farmaco Galidor si basa sull'azione biochimica del suo principio attivo benciclano (N,N-dimetil-3-[[1-(fenilmetil)cicloeptil]ossi]-1-propanamina), che è in grado di modificare l'equilibrio ionico nelle membrane delle cellule muscolari lisce.
Di conseguenza, si avvia il processo di attivazione dell'enzima cellulare ATP-pirofosfato liasi con il contemporaneo blocco delle proteine di membrana, i recettori dell'adenosina. Il risultato di tutte le reazioni biochimiche è una diminuzione delle contrazioni delle cellule del tessuto muscolare viscerale (muscoli degli organi interni). Di conseguenza, si verificano rilassamento muscolare, diminuzione del tono dei vasi sanguigni e riduzione dello spasmo.
Farmacocinetica
Una volta entrato nel tratto gastrointestinale (quando assunto per via orale), il principio attivo di Galidor viene rapidamente assorbito e la sua massima concentrazione plasmatica si raggiunge in media dopo tre ore. Circa il 40% del farmaco si lega alle proteine plasmatiche, fino al 30% agli eritrociti e il 10% ai trombociti.
Dopo il passaggio attraverso il fegato, la biodisponibilità di Halidor (dopo somministrazione orale) è pari al massimo al 35%.
Il benciclano viene metabolizzato nel fegato; i prodotti di degradazione finali vengono escreti nelle urine (emivita compresa tra 6 e 10 ore). La clearance plasmatica del farmaco (clearance totale) è di 40 L all'ora, mentre la clearance renale è inferiore a 1 L all'ora.
Dosaggio e somministrazione
Halidor in compresse per patologie vascolari si assume una compressa (100 mg) tre volte al giorno. La durata media del trattamento è di due mesi, durante i quali il medico può ridurre il dosaggio a una compressa due volte al giorno.
Per alleviare gli spasmi persistenti degli organi interni, si prescrive Galidor in compresse da 100-200 mg una volta al giorno; per la terapia di mantenimento, una compressa tre volte al giorno. La dose massima giornaliera di questo farmaco è di 400 mg e la durata del ciclo terapeutico non supera 1-2 mesi.
Modo di somministrazione di Galidor in soluzione al 2,5%: per via intramuscolare (se necessario per via endovenosa, lentamente) 1-2 ml per iniezione. In caso di patologie vascolari, la soluzione può essere somministrata per infusione (flebo) in vena (4 ml del farmaco vengono diluiti con 100-200 ml di soluzione isotonica di NaCl).
Per gli spasmi degli organi interni, il farmaco viene somministrato per via endovenosa (con soluzione isotonica) o in profondità nel muscolo. Il ciclo di trattamento standard non dura più di tre settimane.
Utilizzare Galidora durante la gravidanza
L'uso di Galidor durante la gravidanza è controindicato. Se Galidor viene prescritto a donne che allattano, l'allattamento al seno deve essere sospeso per tutta la durata dell'assunzione del farmaco.
Controindicazioni
Le controindicazioni all'uso del farmaco Galidor includono: forme gravi di insufficienza respiratoria, renale, epatica e cardiaca scompensata, infarto del miocardio, tachicardia ventricolare, epilessia, ictus emorragico, trauma cranico (subito nell'ultimo anno), età inferiore ai 18 anni.
Effetti collaterali Galidora
Durante l'uso del farmaco Galidor sono possibili i seguenti effetti collaterali: malessere generale, vertigini, mal di testa, secchezza delle fauci, nausea, vomito, diminuzione (o aumento) dell'appetito, dolori addominali, diarrea, tremori, disturbi del sonno.
Sono possibili anche disturbi della memoria simili a crisi epilettiche, disturbi del ritmo cardiaco, aumento di peso e riduzione della conta leucocitaria (leucopenia). Pertanto, l'uso prolungato del farmaco deve essere monitorato per la composizione del sangue.
Durante il trattamento con Galidor, bisogna anche tenere in considerazione la possibilità che questo farmaco abbia un impatto negativo sulla capacità di guidare veicoli e di utilizzare macchinari potenzialmente pericolosi.
Overdose
Il sovradosaggio di Halidor si manifesta con aumento della frequenza cardiaca, diminuzione della pressione sanguigna, minzione spontanea, sonnolenza o ansia; sono possibili collasso e convulsioni. In caso di tali sintomi, è necessario effettuare una lavanda gastrica.
Interazioni con altri farmaci
L'assunzione di Halidor con farmaci che riducono i livelli di potassio (diuretici, lassativi) ne potenzia l'effetto. L'assunzione con glicosidi cardiaci (preparati digitalici) può causare disfunzione cardiaca. L'uso concomitante di Halidor con farmaci per il trattamento dell'aritmia cardiaca o dell'ipertensione arteriosa (beta-bloccanti non selettivi e selettivi) può causare tachicardia.
L'interazione di Halidor con sedativi (calmanti) e anestetici si manifesta nel potenziamento del loro effetto sul sistema nervoso centrale. Inoltre, l'uso di Halidor in concomitanza con l'assunzione di aspirina (acido acetilsalicilico) può compromettere l'aggregazione (l'adesione) delle piastrine e causare emorragie.
 [ 3 ]
[ 3 ]
Condizioni di archiviazione
Questo medicinale appartiene all'elenco B, deve essere conservato in un luogo asciutto, al riparo dalla luce e fuori dalla portata dei bambini, la temperatura ottimale di conservazione è +15-25°C.
Data di scadenza
La durata di conservazione delle compresse di Galidor è di 5 anni, mentre quella della soluzione iniettabile non supera i 3 anni.
Attenzione!
Per semplificare la percezione delle informazioni, questa istruzione per l'utilizzo del farmaco "Halidor" è stata tradotta e presentata in una forma speciale sulla base delle istruzioni ufficiali per l'uso medico del farmaco. Prima dell'uso leggere l'annotazione che è arrivata direttamente al farmaco.
Descrizione fornita a scopo informativo e non è una guida all'autoguarigione. La necessità di questo farmaco, lo scopo del regime di trattamento, i metodi e la dose del farmaco sono determinati esclusivamente dal medico curante. L'automedicazione è pericolosa per la tua salute.

