Esperto medico dell'articolo
Nuove pubblicazioni
Trattamento della sepsi grave e dello shock settico
Last reviewed: 04.07.2025

Tutti i contenuti di iLive sono revisionati o verificati da un punto di vista medico per garantire la massima precisione possibile.
Abbiamo linee guida rigorose in materia di sourcing e colleghiamo solo a siti di media affidabili, istituti di ricerca accademici e, ove possibile, studi rivisti dal punto di vista medico. Nota che i numeri tra parentesi ([1], [2], ecc.) Sono link cliccabili per questi studi.
Se ritieni che uno qualsiasi dei nostri contenuti sia impreciso, scaduto o comunque discutibile, selezionalo e premi Ctrl + Invio.
Un trattamento efficace della sepsi è possibile solo con la completa disinfezione chirurgica del sito di infezione e un'adeguata terapia antimicrobica. Una terapia antimicrobica iniziale inadeguata rappresenta un fattore di rischio di mortalità nei pazienti con sepsi. Mantenere in vita il paziente, prevenire ed eliminare le disfunzioni d'organo è possibile solo con una terapia intensiva mirata.
Il suo obiettivo principale è ottimizzare il trasporto di O2 in condizioni di aumentato consumo, tipiche della sepsi grave e dello shock settico. Questo trattamento si attua attraverso il supporto emodinamico e respiratorio.
Supporto emodinamico
Terapia infusionale
La terapia infusionale è una delle misure iniziali per mantenere l'emodinamica e, soprattutto, la gittata cardiaca. I suoi obiettivi principali nei pazienti con sepsi sono:
- ripristino di una adeguata perfusione tissutale,
- correzione dei disturbi dell'omeostasi,
- normalizzazione del metabolismo cellulare,
- riduzione della concentrazione di mediatori della cascata settica e di metaboliti tossici.
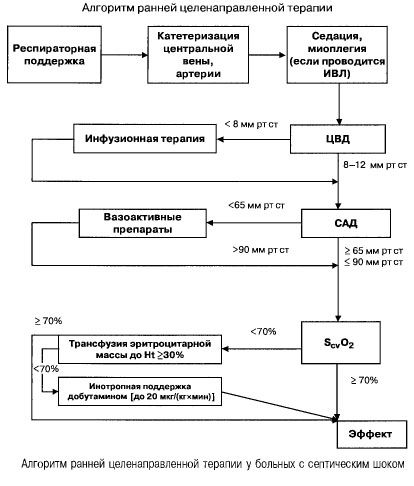
Nella sepsi con insufficienza multiorgano e shock settico, si cerca di raggiungere rapidamente (entro le prime 6 ore) i seguenti valori di indicatori importanti:
- ematocrito >30%,
- diuresi 0,5 ml/(kgh),
- saturazione del sangue nella vena cava superiore o nell'atrio destro >70%,
- pressione sanguigna media >65 mm Hg,
- PVC 8-12 mm Hg
Il mantenimento di questi valori al livello specificato migliora la sopravvivenza del paziente (categoria di evidenza B). Il monitoraggio emodinamico mediante catetere Swan-Ganz e la tecnologia PICCO (termodiluizione transpolmonare e analisi dell'onda di polso) ampliano le possibilità di monitoraggio e valutazione dell'efficacia della terapia emodinamica, ma non vi sono prove che migliorino la sopravvivenza.
Il valore di precarico ottimale viene selezionato individualmente, poiché è necessario tenere conto del grado di danno endoteliale e dello stato del drenaggio linfatico nei polmoni, della funzione diastolica dei ventricoli e delle variazioni della pressione intratoracica. Il volume della terapia infusionale viene selezionato in modo che la PCWP non superi la COP plasmatica (prevenzione della OL) e si verifichi un aumento della CO. Inoltre, vengono presi in considerazione i parametri che caratterizzano la funzione di scambio gassoso dei polmoni (paO2 e paO2 / FiO2 ) e le variazioni del quadro radiografico.
Per la terapia infusionale nell'ambito del trattamento mirato della sepsi e dello shock settico, si utilizzano soluzioni cristalloidi e colloidali con risultati praticamente identici.
Tutti i mezzi di infusione presentano vantaggi e svantaggi. Oggi, alla luce dei risultati di studi sperimentali e clinici, non vi è motivo di preferire un tipo in particolare.
- Ad esempio, per un'adeguata correzione del ritorno venoso e del livello di precarico, è necessario somministrare un volume di cristalloidi 2-4 volte superiore a quello dei colloidi, il che è associato alle peculiarità della distribuzione della soluzione nell'organismo. Inoltre, l'infusione di cristalloidi è associata a un maggiore rischio di edema tissutale e il loro effetto emodinamico è più breve rispetto a quello dei colloidi. Allo stesso tempo, i cristalloidi sono più economici, non influenzano il potenziale coagulativo e non provocano reazioni anafilattoidi. Sulla base di quanto sopra, la composizione qualitativa del programma di infusione viene determinata in base alle caratteristiche del paziente, tenendo conto del grado di ipovolemia, della fase della sindrome DIC, della presenza di edema periferico e della concentrazione di albumina nel siero, nonché della gravità del danno polmonare acuto.
- I sostituti del plasma (destrani, preparati di gelatina, amido idrossietilico) sono indicati in caso di grave deficit di BCC. Gli amidi idrossietilici con un grado di sostituzione di 200/0,5, 130/0,4 e 130/0,42 presentano un potenziale vantaggio rispetto ai destrani grazie a un minor rischio di fuoriuscita di membrana e all'assenza di un effetto clinicamente significativo sull'emostasi.
- L'introduzione di albumina in condizioni critiche può aumentare il rischio di morte. L'aumento della pressione arteriosa polmonare (COP) durante la sua infusione è transitorio e, in seguito, in condizioni di aumentata permeabilità del letto capillare (sindrome da "perdita capillare"), si verifica un'ulteriore stravasazione di albumina. È possibile che la trasfusione di albumina sia utile solo se la sua concentrazione nel siero è inferiore a 20 g/l e non vi sono segni di "perdita" nell'interstizio.
- L'uso del crioplasma è indicato in caso di coagulopatia da consumo e diminuzione del potenziale coagulativo del sangue.
- L'uso diffuso di eritrociti di donatori dovrebbe essere limitato a causa dell'elevato rischio di sviluppare diverse complicazioni (leucemia prostatica benigna, reazioni anafilattiche, ecc.). Secondo la maggior parte degli esperti, la concentrazione minima di emoglobina nei pazienti con sepsi grave è di 90-100 g/l.
Correzione dell'ipotensione
Una bassa pressione di perfusione richiede l'attivazione immediata di farmaci che aumentano il tono vascolare e/o la funzione inotropa del cuore. La dopamina o la noradrenalina sono i farmaci di prima linea per la correzione dell'ipotensione nei pazienti con shock settico.
La dopamina (dopmin) a una dose <10 mcg/(kg x min) aumenta la pressione arteriosa (PA), principalmente aumentando la gittata cardiaca (CO), e ha un effetto minimo sulle resistenze vascolari sistemiche. A dosi elevate, il suo effetto α-adrenergico predomina, inducendo vasocostrizione arteriosa, e a una dose <5 mcg/(kg x min) la dopamina stimola i recettori dopaminergici dei vasi renali, mesenterici e coronarici, inducendo vasodilatazione, aumento della filtrazione glomerulare ed escrezione di Na+.
La noradrenalina aumenta la pressione arteriosa media e la filtrazione glomerulare. L'ottimizzazione dell'emodinamica sistemica sotto la sua azione porta a un miglioramento della funzione renale senza l'uso di basse dosi di dopamina. Studi condotti negli ultimi anni hanno dimostrato che il suo uso isolato, rispetto a una combinazione con alte dosi di dopamina, porta a una riduzione statisticamente significativa della mortalità.
L'adrenalina è un farmaco adrenergico con gli effetti collaterali emodinamici più pronunciati. Ha un effetto dose-dipendente su frequenza cardiaca, pressione arteriosa media, gittata cardiaca, funzione ventricolare sinistra e apporto e consumo di O2 . Tuttavia, tachiaritmie, deterioramento del flusso ematico d'organo e iperlattatemia si verificano contemporaneamente. Pertanto, l'uso dell'adrenalina è limitato ai casi di completa refrattarietà ad altre catecolamine.
La dobutamina è il farmaco di scelta per aumentare l'apporto e il consumo di CO e O2 a precarico normale o elevato. Grazie alla sua azione predominante sui recettori beta1-adrenergici, è più efficace della dopamina nell'aumentare questi parametri.
Studi sperimentali hanno dimostrato che le catecolamine, oltre a supportare la circolazione sanguigna, possono regolare il decorso dell'infiammazione sistemica influenzando la sintesi di mediatori chiave con un effetto a distanza. Sotto l'influenza di adrenalina, dopamina, noradrenalina e dobutamina, i macrofagi attivati riducono la sintesi e la secrezione di TNF-α.
La selezione degli agenti adrenergici viene effettuata secondo il seguente algoritmo:
- indice cardiaco 3,5-4 l/(min x m 2 ), SvO 2 >70% - dopamina o noradrenalina,
- indice cardiaco <3,5 l/(min x m 2 ), SvO 2 <70% - dobutamina (se pressione arteriosa sistolica <70 mm Hg - insieme a noradrenalina o dopamina).
 [ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ]
[ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ]
Supporto respiratorio
I polmoni sono tra i primi organi bersaglio coinvolti nel processo patologico della sepsi. L'insufficienza respiratoria acuta è una delle principali componenti della disfunzione multiorgano. Le sue manifestazioni cliniche e di laboratorio nella sepsi corrispondono all'ALI e, con la progressione del processo patologico, all'ARDS. Le indicazioni alla ventilazione meccanica nella sepsi grave sono determinate in base alla gravità dell'insufficienza respiratoria parenchimatosa (IRA o ARDS). Il suo criterio è l'indice respiratorio:
- <200 - sono indicati l'intubazione tracheale e il supporto respiratorio,
- >200 - le letture vengono determinate individualmente.
Se il paziente è cosciente durante la respirazione spontanea con supporto di ossigeno, non vi è un elevato dispendio di lavoro respiratorio e una tachicardia marcata (FC <120 al minuto), e il valore normale di SO2 di ritorno venoso è >90%, è possibile evitare il trasferimento alla ventilazione artificiale. Tuttavia, è necessario monitorare attentamente le condizioni del paziente. Il valore ottimale di SO2 è circa il 90%. Può essere mantenuto con vari metodi di somministrazione di gas (maschere facciali, cateteri nasali) a concentrazioni non tossiche (FiO2 < 0,6). La ventilazione artificiale non invasiva è controindicata in caso di sepsi (categoria di evidenza B).
Le modalità di ventilazione meccanica ad alto volume (MVV) (VO2 = 12 ml/kg) dovrebbero essere evitate, poiché in tali casi la secrezione di citochine da parte dei polmoni aumenta, con conseguente aggravamento della MOF. È necessario aderire al concetto di ventilazione meccanica sicura, possibile se sono soddisfatte le seguenti condizioni (categoria di evidenza A):
- OD <10 ml/kg,
- rapporto non invertito tra inspirazione ed espirazione,
- pressione massima delle vie aeree <35 cm H2O,
- FiO 2 <0,6.
La selezione dei parametri del ciclo respiratorio viene effettuata fino al raggiungimento di una ventilazione meccanica adeguata; i suoi criteri sono paO2 > 60 mm Hg, SpO2 > 88-93%, pvO2 35-45 mm Hg, SvO2 > 55%.
Uno dei metodi efficaci per ottimizzare lo scambio gassoso è la ventilazione artificiale in posizione prona (Prone Positioning) (categoria di evidenza B). Questa posizione è efficace nei pazienti nelle condizioni più gravi, sebbene il suo effetto sulla riduzione della mortalità a lungo termine sia statisticamente insignificante.
Supporto nutrizionale
L'esecuzione di un supporto nutrizionale artificiale è un elemento importante del trattamento, una delle misure obbligatorie, poiché lo sviluppo della sindrome da insufficienza multiorgano nella sepsi è solitamente accompagnato da manifestazioni di ipermetabolismo. In tale situazione, il fabbisogno energetico viene soddisfatto dalla distruzione delle proprie strutture cellulari (autocannibalismo), che aggrava la disfunzione d'organo e aumenta l'endotossicosi.
Il supporto nutrizionale è considerato un metodo per prevenire l'esaurimento grave (carenza proteico-energetica) in presenza di un marcato aumento del catabolismo e del metabolismo. L'inclusione della nutrizione enterale nel complesso della terapia intensiva previene la migrazione della microflora intestinale, la disbatteriosi, aumenta l'attività funzionale degli enterociti e le proprietà protettive della mucosa intestinale. Questi fattori riducono il grado di endotossicosi e il rischio di complicanze infettive secondarie.
Calcolo del supporto nutrizionale:
- valore energetico - 25-35 kcal/(kg di peso corporeo x giorno),
- quantità di proteine - 1,3-2,0 g/(kg di peso corporeo x giorno),
- quantità di carboidrati (glucosio) - inferiore a 6 g/kg/giorno,
- quantità di grassi - 0,5-1 g/kg/giorno,
- dipeptidi di glutammina 0,3-0,4 g/kg/giorno,
- vitamine - dose giornaliera standard + vitamina K (10 mg/giorno) + vitamine B 1 e B 6 (100 mg/giorno) + vitamine A, C, E,
- microelementi - dose giornaliera standard + Zn (15-20 mg/die + 10 mg/die in presenza di feci molli),
- elettroliti - Na+, K+, Ca2+ secondo calcoli di bilancio e concentrazione nel plasma.
L'inizio precoce del supporto nutrizionale (24-36 ore) è più efficace rispetto al 3°-4° giorno di terapia intensiva (categoria di evidenza B), soprattutto in caso di alimentazione enterale tramite sondino.
Nella sepsi grave, non vi sono vantaggi derivanti dalla nutrizione enterale o parenterale; la durata della disfunzione d'organo e la durata del supporto respiratorio e inotropo sono le stesse, così come i tassi di mortalità. Considerato quanto sopra, la nutrizione enterale precoce rappresenta un'alternativa più economica alla nutrizione parenterale. L'uso di miscele arricchite con fibre alimentari (prebiotici) per l'alimentazione tramite sondino riduce significativamente l'incidenza di diarrea nei pazienti con sepsi grave.
Per un'efficace sintesi proteica nell'organismo, è importante mantenere il rapporto metabolico "azoto totale, g - calorie non proteiche, kcal" = 1-(110-130). La dose massima di carboidrati è di 6 g / (kg di peso corporeo al giorno), poiché l'introduzione di dosi elevate rischia di causare iperglicemia e l'attivazione del catabolismo nei muscoli scheletrici. Si raccomanda la somministrazione di emulsioni lipidiche 24 ore su 24.
Controindicazioni al supporto nutrizionale:
- acidosi metabolica scompensata,
- intolleranza individuale ai supporti nutrizionali,
- grave ipovolemia non recuperata,
- shock refrattario - dose di dopamina >15 mcg/(kg x min) e pressione sanguigna sistolica <90 mm Hg,
- grave ipossiemia arteriosa intrattabile.
Controllo glicemico
Un aspetto importante del trattamento complesso della sepsi grave è il monitoraggio costante della concentrazione di glucosio nel plasma e la terapia insulinica. Una glicemia elevata e la necessità di correggerla sono fattori di esito sfavorevole nella sepsi. Date le circostanze sopra descritte, nei pazienti viene mantenuta una normoglicemia (4,5-6,1 mmol/l) per la quale, quando la concentrazione di glucosio supera i valori accettabili, viene eseguita un'infusione di insulina (0,5-1 U/h). A seconda della situazione clinica, la concentrazione di glucosio viene monitorata ogni 1-4 ore. L'implementazione di questo algoritmo ha evidenziato un aumento statisticamente significativo della sopravvivenza dei pazienti.
 [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ]
[ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ]
Glucocorticoidi
I risultati degli studi moderni riguardanti l'efficacia dell'uso dei glucocorticoidi nei pazienti con shock settico sono riassunti nelle seguenti affermazioni:
- non è appropriato usare ormoni ad alte dosi [metilprednisolone 30-120 mg/(kg x giorno) una volta o per 9 giorni, desametasone 2 mg/(kg x giorno) per 2 giorni, betametasone 1 mg/(kg x giorno) per 3 giorni] - aumento del rischio di infezioni ospedaliere, nessun effetto sulla sopravvivenza,
- L'uso di idrocortisone alla dose di 240-300 mg al giorno per 5-7 giorni accelera la stabilizzazione dei parametri emodinamici, consente la sospensione del supporto vascolare e migliora la sopravvivenza nei pazienti con concomitante insufficienza surrenalica relativa (categoria di evidenza B).
È necessario abbandonare la caotica prescrizione empirica di prednisolone e desametasone: non vi sono motivi per estrapolare nuove informazioni su di essi. In assenza di evidenze di laboratorio di insufficienza surrenalica relativa, si somministra idrocortisone alla dose di 300 mg al giorno (in 3-6 iniezioni).
- nello shock refrattario,
- se sono necessarie dosi elevate di vasopressori per mantenere un'emodinamica efficace.
È possibile che in condizioni di infiammazione sistemica in shock settico, l'efficacia dell'idrocortisone sia associata all'attivazione dell'inibitore del fattore nucleare kB (NF-kB-α) e alla correzione dell'insufficienza surrenalica relativa. A sua volta, l'inibizione dell'attività del fattore nucleare di trascrizione (NF-kB) porta a una riduzione della formazione di NO sintetasi inducibile (NO è il più potente vasodilatatore endogeno), citochine proinfiammatorie, COX e molecole di adesione.
Proteina C attivata
Una delle manifestazioni caratteristiche della sepsi è l'interruzione della coagulazione sistemica (attivazione della cascata coagulativa e inibizione della fibrinolisi), che in ultima analisi porta a ipoperfusione e disfunzione d'organo. L'effetto della proteina C attivata sul sistema infiammatorio si manifesta in diversi modi:
- riduzione dell'adesione della selectina ai leucociti, che protegge l'endotelio dai danni, che svolge un ruolo chiave nello sviluppo dell'infiammazione sistemica,
- riduzione del rilascio di citochine dai monociti,
- bloccando il rilascio di TNF-a dai leucociti,
- inibizione della produzione di trombina (potenzia la risposta infiammatoria).
Azione anticoagulante, profibrinolitica e antinfiammatoria
- la proteina C attivata è dovuta a
- degradazione dei fattori Va e VIIIa - soppressione della formazione di trombi,
- soppressione dell'inibitore dell'attivatore del plasminogeno - attivazione della fibrinolisi,
- effetto antinfiammatorio diretto sulle cellule endoteliali e sui neutrofili,
- protezione dell'endotelio dall'apoptosi
La somministrazione di proteina C attivata [drotrecogin alfa (attivata)] a 24 mcg/(kg h) per 96 h riduce il rischio di morte del 19,4%. Indicazioni per la somministrazione: sepsi con MOF acuta ed elevato rischio di morte (APACHE II > 25 punti, disfunzione di 2 o più organi, categoria di evidenza B).
La proteina C attivata non riduce la mortalità nei bambini, nei pazienti con disfunzione monoorgano, APACHE II < 25 punti, nei pazienti con sepsi non chirurgica.
 [ 14 ], [ 15 ], [ 16 ], [ 17 ]
[ 14 ], [ 15 ], [ 16 ], [ 17 ]
Immunoglobuline
L'opportunità della somministrazione endovenosa di immunoglobuline (IgG e IgG+IgM) è associata alla loro capacità di limitare l'azione eccessiva delle citochine proinfiammatorie, aumentare la clearance delle endotossine e del superantigene stafilococcico, eliminare l'anergia e potenziare l'effetto degli antibiotici ß-lattamici. Il loro utilizzo nel trattamento della sepsi grave e dello shock settico è l'unico metodo di immunocorrezione che aumenta la sopravvivenza. L'effetto migliore è stato registrato con l'utilizzo di una combinazione di IgG e IgM [RR=0,48 (0,35-0,75), categoria di evidenza A]. Il regime posologico standard è di 3-5 ml/(kg x die) per 3 giorni consecutivi. Con l'utilizzo di immunoglobuline, i risultati più ottimali sono stati ottenuti nella fase precoce dello shock ("shock caldo") e nei pazienti con sepsi grave (punteggio APACHE II di 20-25 punti).
Prevenzione della trombosi venosa profonda
La prevenzione della TVP degli arti inferiori influisce significativamente sugli esiti del trattamento nei pazienti con sepsi (categoria di evidenza A). A tale scopo vengono utilizzate sia le eparine non frazionate che le eparine a basso peso molecolare. I principali vantaggi delle eparine a basso peso molecolare sono una minore incidenza di complicanze emorragiche, un effetto più debole sulla funzionalità piastrinica e un effetto prolungato (possono essere somministrate una volta al giorno).
Prevenzione della formazione di ulcere da stress del tratto gastrointestinale
Questa direzione gioca un ruolo significativo nel raggiungimento di un esito favorevole nel trattamento dei pazienti con sepsi grave e shock settico, poiché il tasso di mortalità per emorragia da ulcere da stress del tratto gastrointestinale è del 64-87%. Senza misure preventive, le ulcere da stress si verificano nel 52,8% dei pazienti critici. Tuttavia, l'uso di inibitori della pompa protonica e bloccanti dei recettori H2 dell'istamina riduce il rischio di oltre 2 volte (il primo gruppo di farmaci è più efficace del secondo). La principale direzione di prevenzione e trattamento è il mantenimento del pH tra 3,5 e 6,0. Va sottolineato che, oltre ai farmaci sopra menzionati, la nutrizione enterale svolge un ruolo importante nella prevenzione della formazione di ulcere da stress.
Purificazione extracorporea del sangue
Diverse sostanze biologicamente attive e prodotti metabolici coinvolti nello sviluppo dell'infiammazione generalizzata sono target per i metodi di disintossicazione, il che è particolarmente importante in assenza di clearance epatorenale naturale in condizioni di insufficienza multiorgano. I metodi di terapia sostitutiva renale sono considerati promettenti, in quanto possono influenzare non solo i disturbi uremici nei pazienti con insufficienza renale, ma anche avere un effetto positivo su altre alterazioni dell'omeostasi e disfunzioni d'organo che si verificano in caso di sepsi, shock e insufficienza multiorgano.
Ad oggi, non esistono dati che confermino la necessità di utilizzare metodi di purificazione extracorporea del sangue come una delle principali direzioni della terapia patogenetica della sepsi e dello shock settico. Il loro utilizzo è giustificato in caso di insufficienza multiorgano con predominanza renale.
 [ 18 ], [ 19 ], [ 20 ], [ 21 ], [ 22 ], [ 23 ]
[ 18 ], [ 19 ], [ 20 ], [ 21 ], [ 22 ], [ 23 ]
Emodialisi
L'essenza del metodo è la diffusione di sostanze a basso peso molecolare (fino a 5x10 3 Da) attraverso una membrana semipermeabile e la rimozione del fluido in eccesso dal corpo lungo un gradiente di pressione. L'emodialisi è ampiamente utilizzata per trattare pazienti con insufficienza renale sia cronica che acuta. La velocità di diffusione delle sostanze dipende esponenzialmente dal loro peso molecolare. Ad esempio, la rimozione degli oligopeptidi è più lenta della loro sintesi.
Emofiltrazione
L'emofiltrazione è un metodo efficace per rimuovere sostanze con un peso molecolare di 5x10 3 - 5x10 4 Da ed è l'unico modo per rimuovere dall'organismo un ampio gruppo di sostanze e metaboliti biologicamente attivi. Il metodo si basa sul metodo di trasferimento di massa per convezione. Oltre a un'adeguata correzione dell'azotemia, l'emofiltrazione rimuove efficacemente anafilotossine C3a, C5a, citochine proinfiammatorie (TNF-α, IL-1b, 6 e 8), β2-microglobulina, mioglobina, ormone paratiroideo, lisozima (peso molecolare - 6000 Da), α-amilasi (peso molecolare - 36.000-51.000 Da), creatinfosfochinasi, fosfatasi alcalina, transaminasi e altre sostanze. L'emofiltrazione rimuove amminoacidi e proteine plasmatiche (incluse immunoglobuline e immunocomplessi circolanti).
Emodiafiltrazione
L'emodiafiltrazione è il metodo più potente di purificazione del sangue, che combina diffusione e convezione (ovvero GD e GF). Un ulteriore contributo al processo di detossificazione è dato dall'assorbimento delle sostanze patologiche sulla membrana filtrante.
Plasmaferesi
La plasmaferesi (plasmaferesi, filtrazione plasmatica) è considerata anche un possibile metodo per correggere l'infiammazione generalizzata nei pazienti con sepsi e shock settico. Il metodo ottimale è considerato l'utilizzo della plasmaferesi in modalità continua con la rimozione di 3-5 volumi di plasma e la sua contemporanea sostituzione con soluzioni fresche congelate, di albumina, colloidali e cristalloidi. Con un coefficiente di setacciatura pari a 1, la filtrazione plasmatica garantisce una buona rimozione di proteina C-reattiva, aptoglobina, frammento C3 del complemento, 1-antitripsina, IL-6, trombossano-B2, fattore stimolante i granulociti, TNF. L'uso di sorbenti per purificare il plasma del paziente riduce il rischio di infezione e i costi della procedura, poiché non è necessario l'utilizzo di proteine estranee.
L'uso dell'infusione prolungata di selenito di sodio (selenasi) 1000 mcg/giorno nella sepsi grave porta a una riduzione della mortalità.
Il selenio è un microelemento essenziale, la cui importanza è legata al suo ruolo chiave nei sistemi antiossidanti delle cellule. Il livello di selenio nel sangue è mantenuto tra 1,9 e 3,17 μM/l. Il fabbisogno di selenio è di 50-200 μg al giorno e dipende dalla disponibilità di altri antiossidanti e microelementi.
Il selenio è un potente antiossidante, componente della glutatione perossidasi, della fosfolina glutatione perossidasi, di altre ossidoreduttasi e di alcune transferasi. La glutatione perossidasi è l'anello più importante del sistema antiossidante endogeno.
L'efficacia del selenio in condizioni critiche è stata studiata negli ultimi anni. Questi studi hanno dimostrato che i principali meccanismi d'azione del selenio sono:
- soppressione dell'iperattivazione di NF-kB;
- diminuzione dell'attivazione del complemento;
- la sua azione come immunomodulatore, antiossidante e antinfiammatorio
- mantenimento dell'utilizzo del perossido;
- soppressione dell'adesione endoteliale (ridotta espressione di ICAM-1, VCAM-2,
- E - selectina, P - selectina);
- protezione dell'endotelio dai radicali ossigeni (mediante la selenoproteina P, che impedisce la formazione di perossinitrito da O2 e NO).
Riassumendo quanto sopra, possiamo definire i compiti specifici della terapia intensiva per la sepsi grave:
- Supporto emodinamico: PVC 8-12 mm Hg, PA media >65 mm Hg, diuresi 0,5 ml/(kg h), ematocrito >30%, saturazione nel sangue venoso misto >70%.
- Supporto respiratorio: pressione di picco delle vie aeree <35 cm H2O, frazione inspiratoria di ossigeno <60%, volume corrente <10 ml/kg, rapporto inspiratorio/espiratorio non invertito.
- Glucocorticoidi - "basse dosi" (idrocortisone 240-300 mg al giorno).
- Proteina C attivata 24 mcg/(kg h) per 4 giorni in caso di sepsi grave (APACHE II >25).
- Terapia sostitutiva immunocorrettiva con pentaglobina.
- Prevenzione della trombosi venosa profonda degli arti inferiori.
- Prevenzione della formazione di ulcere da stress del tratto gastrointestinale: uso di inibitori della pompa protonica e bloccanti del recettore H2-istamina.
- Terapia sostitutiva per l'insufficienza renale acuta.
- Supporto nutrizionale: valore energetico degli alimenti 25-30 kcal/kg di peso corporeo x giorno), proteine 1,3-2,0 g/(kg di peso corporeo x giorno), dipeptidi di glutammina 0,3-0,4 g/(kg x giorno), glucosio - 30-70% delle calorie non proteiche, a condizione che la glicemia sia mantenuta <6,1 mmol/l, grassi - 15-50% delle calorie non proteiche.

