Ghiandole paratiroidi
Last reviewed: 25.06.2018

Abbiamo rigide linee guida per la selezione delle fonti e rimandiamo solo a siti medici affidabili, istituti di ricerca accademica e, ove possibile, a studi sottoposti a revisione paritaria. Si noti che i numeri tra parentesi ([1], [2], ecc.) sono link cliccabili a questi studi.
Se ritieni che uno qualsiasi dei nostri contenuti sia inaccurato, obsoleto o comunque discutibile, selezionalo e premi Ctrl + Invio.

Nel 1879, lo scienziato svedese S. Sandström descrisse le paratiroidi negli esseri umani e diede loro un nome. Le paratiroidi sono organi vitali. La loro funzione è quella di produrre e secernere l'ormone paratiroideo (PTH), uno dei principali regolatori del metabolismo del calcio e del fosforo.
Le paratiroidi pari superiori (glandula paratiroidea superior) e inferiori (glandula paratiroidea inferior) sono corpi rotondi od ovoidali situati sulla superficie posteriore di ciascun lobo della tiroide: una ghiandola in alto, l'altra in basso. La lunghezza di ciascuna ghiandola è di 4-8 mm, la larghezza di 3-4 mm, lo spessore di 2-3 mm. Il numero di queste ghiandole non è costante e può variare da 2 a 7-8, in media ce ne sono quattro. La massa totale delle ghiandole è in media di 1,18 g.
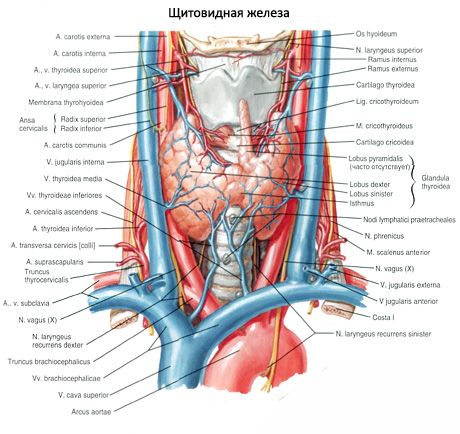
Le paratiroidi differiscono dalla tiroide per il loro colore più chiaro (nei bambini sono rosa pallido, negli adulti - marrone-giallastro). Spesso le paratiroidi si trovano nel sito di penetrazione del tessuto tiroideo da parte delle arterie tiroidee inferiori o dei loro rami. Le paratiroidi sono separate dai tessuti circostanti da una propria capsula fibrosa, dalla quale si estendono strati di tessuto connettivo all'interno delle ghiandole. Questi contengono un gran numero di vasi sanguigni e dividono le paratiroidi in gruppi di cellule epiteliali.
Il parenchima delle ghiandole è formato dai paratiroidi principali e acidofili, che formano cordoni e gruppi circondati da sottili fasci di fibre di tessuto connettivo. Entrambi i tipi di cellule sono considerati stadi diversi dello sviluppo dei paratiroidi. I paratiroidi principali hanno una forma poliedrica, un citoplasma basofilo con un gran numero di ribosomi. Tra queste cellule si distinguono le cellule scure (che secernono attivamente) e quelle chiare (meno attive). I paratiroidi acidofili sono grandi, con contorni chiari e contengono molti piccoli mitocondri con particelle di glicogeno.
L'ormone delle paratiroidi, la paratiroxina (paratormone), è di composizione proteica e partecipa alla regolazione del metabolismo fosforo-calcio. Il paratiroide riduce l'escrezione di calcio nelle urine e ne aumenta l'assorbimento intestinale in presenza di vitamina D. La tireocalcitonina è un antagonista del paratiroide.
Embriogenesi delle paratiroidi
Le paratiroidi si sviluppano dall'epitelio delle tasche branchiali III e IV pari. Nella settima settimana di sviluppo, i rudimenti epiteliali dei corpi si separano dalle pareti delle tasche branchiali e, durante la crescita, si muovono in direzione caudale. Successivamente, le paratiroidi in formazione occupano una posizione permanente sulle superfici posteriori dei lobi destro e sinistro della tiroide.
 [ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ]
[ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ]
Vasi e nervi delle ghiandole paratiroidi
L'afflusso di sangue alle paratiroidi è garantito dai rami delle arterie tiroidee superiore e inferiore, nonché dai rami esofageo e tracheale. Il sangue venoso scorre attraverso le vene omonime. L'innervazione delle paratiroidi è simile a quella della tiroide.
Caratteristiche delle paratiroidi legate all'età
La massa totale delle paratiroidi in un neonato oscilla tra 6 e 9 mg. Durante il primo anno di vita, la loro massa totale aumenta di 3-4 volte, all'età di 5 anni raddoppia nuovamente e all'età di 10 anni triplica. Dopo 20 anni, la massa totale delle quattro paratiroidi raggiunge i 120-140 mg e rimane costante fino all'età avanzata. A tutte le età, la massa delle paratiroidi nelle donne è leggermente maggiore rispetto agli uomini.
Di solito, una persona ha due paia di paratiroidi (superiori e inferiori), situate sulla superficie posteriore della tiroide, all'esterno della sua capsula, vicino ai poli superiore e inferiore. Tuttavia, il numero e la localizzazione delle paratiroidi possono variare; a volte si trovano fino a 12 paratiroidi. Possono essere localizzate nel tessuto della tiroide e del timo, nel mediastino anteriore e posteriore, nel pericardio, dietro l'esofago, nella zona della biforcazione dell'arteria carotide. Le paratiroidi superiori hanno la forma di un ovoide appiattito, quelle inferiori sono sferiche. Le loro dimensioni sono approssimativamente da 6x3 a 4x1,5 - 3 mm, il peso totale è da 0,05 a 0,5 g, il colore è rossastro o giallo-marrone. L'afflusso di sangue alle paratiroidi è assicurato principalmente dai rami dell'arteria tiroidea inferiore, mentre il deflusso venoso avviene attraverso le vene della tiroide, dell'esofago e della trachea. Le paratiroidi sono innervate dalle fibre simpatiche dei nervi laringei ricorrenti e superiori, mentre l'innervazione parasimpatica è assicurata dai nervi vaghi. Le paratiroidi sono rivestite da una sottile capsula di tessuto connettivo; i setti che si estendono da questa penetrano nelle ghiandole. Contengono vasi sanguigni e fibre nervose. Il parenchima delle paratiroidi è costituito da paratiroidi, o cellule principali, tra cui, a seconda del grado di colorazione, si distinguono cellule chiare o lucide ormonalmente attive, nonché cellule scure quiescenti. Le cellule principali formano gruppi, cordoni e gruppi e, negli anziani, follicoli con colloide nella cavità. Negli adulti, compaiono cellule, localizzate principalmente lungo la periferia delle paratiroidi, colorate con eosina: cellule eosinofile o ossifile, che sono cellule principali in degenerazione. Nelle paratiroidi si possono trovare anche forme di transizione tra le cellule principali e le ossifile.
I primi successi nel chiarire le questioni relative alla sintesi, alla decodificazione della struttura e allo studio del metabolismo dell'ormone paratiroideo furono ottenuti dopo il 1972. L'ormone paratiroideo è un polipeptide a catena singola costituito da 84 residui amminoacidici, privo di cisteina, con un peso molecolare di circa 9500 dalton, formato nelle paratiroidi da un bioprecursore, l'ormone proparatiroideo (proPTH), che presenta altri 6 amminoacidi all'estremità NH₂ . Il proPTH viene sintetizzato nelle cellule principali delle paratiroidi (nel loro reticolo endoplasmatico granulare) e, tramite scissione proteolitica nell'apparato di Golgi, viene convertito in ormone paratiroideo. La sua attività biologica è significativamente inferiore a quella del PTH. Apparentemente, il proPTH è assente nel sangue delle persone sane, ma in condizioni patologiche (con adenoma delle paratiroidi) può essere secreto nel sangue insieme al PTH. Recentemente, è stato scoperto un precursore del proPTH, il preproPTH, che contiene 25 residui amminoacidici aggiuntivi all'estremità NH2-terminale. Pertanto, il preproPTH contiene 115 residui amminoacidici, il proPTH 90 e il PTH 84.
La struttura dell'ormone paratiroideo bovino e suino è stata ormai completamente definita. L'ormone paratiroideo umano è stato isolato da adenomi delle paratiroidi, ma la sua struttura è stata solo parzialmente decifrata. Esistono differenze nella struttura dell'ormone paratiroideo, ma gli ormoni paratiroidei animali e umani mostrano immunoreattività crociata. Il polipeptide costituito dai primi 34 residui amminoacidici conserva praticamente l'attività biologica dell'ormone naturale. Ciò ci permette di supporre che la restante percentuale di circa il 50% della molecola all'estremità carbossilica non sia direttamente correlata agli effetti principali dell'ormone paratiroideo. Anche i frammenti 1-29 dell'ormone paratiroideo mostrano una certa attività biologica e immunologica. Anche i frammenti biologicamente inattivi 53-84 mostrano un effetto immunologico, ovvero queste proprietà dell'ormone paratiroideo sono espresse da almeno 2 sezioni della sua molecola.
L'ormone paratiroideo circolante nel sangue è eterogeneo e differisce dall'ormone nativo secreto dalle paratiroidi. Nel sangue si distinguono almeno tre diversi tipi di ormone paratiroideo: ormone paratiroideo intatto con un peso molecolare di 9.500 dalton; sostanze biologicamente inattive derivanti dalla parte carbossilica della molecola di ormone paratiroideo con un peso molecolare di 7.000-7.500 dalton; sostanze biologicamente attive con un peso molecolare di circa 4.000 dalton.
Frammenti ancora più piccoli sono stati trovati nel sangue venoso, a indicare che si erano formati in periferia. Gli organi principali in cui si formavano frammenti di ormone paratiroideo erano il fegato e i reni. La frammentazione dell'ormone paratiroideo in questi organi era aumentata nelle patologie epatiche e nell'insufficienza renale cronica (IRC). In queste condizioni, i frammenti dell'ormone paratiroideo rimanevano nel flusso sanguigno significativamente più a lungo rispetto agli individui sani. Il fegato assorbiva principalmente l'ormone paratiroideo intatto, ma non rimuoveva dal sangue né i frammenti carbossi-terminali né quelli amino-terminali. I reni svolgevano un ruolo fondamentale nel metabolismo dell'ormone paratiroideo. Rappresentavano quasi il 60% della clearance metabolica dell'ormone immunoreattivo carbossi-terminale e il 45% del frammento amino-terminale dell'ormone paratiroideo. L'area principale del metabolismo del frammento amino-terminale attivo dell'ormone paratiroideo era l'osso.
È stata rilevata una secrezione pulsante di ormone paratiroideo, più intensa durante la notte. Dopo 3-4 ore dall'inizio del sonno notturno, il suo contenuto nel sangue è 2,5-3 volte superiore al livello medio diurno.
La funzione principale del paratormone è quella di mantenere l'omeostasi del calcio. Allo stesso tempo, il calcio sierico (totale e soprattutto ionizzato) è il principale regolatore della secrezione del paratormone (una diminuzione dei livelli di calcio stimola la secrezione del paratormone, mentre un aumento la inibisce), ovvero la regolazione avviene secondo il principio del feedback. In condizioni di ipocalcemia, la conversione del proPTH in paratormone aumenta. Anche il contenuto di magnesio nel sangue svolge un ruolo importante nel rilascio del paratormone (un suo aumento stimola la secrezione del paratormone, mentre una sua diminuzione la inibisce). I principali bersagli del paratormone sono i reni e le ossa scheletriche, ma è noto l'effetto del paratormone sull'assorbimento intestinale del calcio, sulla tolleranza ai carboidrati, sui livelli sierici dei lipidi, sul suo ruolo nello sviluppo dell'impotenza, del prurito cutaneo, ecc.
Per caratterizzare l'effetto dell'ormone paratiroideo sulle ossa, è necessario fornire brevi informazioni sulla struttura del tessuto osseo e sulle caratteristiche del suo riassorbimento fisiologico e del suo rimodellamento.
È noto che la maggior parte del calcio presente nell'organismo (fino al 99%) è contenuta nel tessuto osseo. Poiché si trova nelle ossa sotto forma di composti fosforo-calcio, il 99% del contenuto totale di fosforo si trova anche nelle ossa. Il loro tessuto, nonostante la sua apparente natura statica, è in costante rimodellamento, attivamente vascolarizzato e possiede elevate proprietà meccaniche. L'osso è un "deposito" dinamico di fosforo, magnesio e altri composti necessari per mantenere l'omeostasi del metabolismo minerale. La sua struttura comprende componenti minerali densi strettamente correlati alla matrice organica, costituita per il 90-95% da collagene, piccole quantità di mucopolisaccaridi e proteine non collageniche. La componente minerale dell'osso è costituita da idrossiapatite - la cui formula empirica è Ca₂O(PO₂)₁(OH)₂ - e fosfato di calcio amorfo.
L'osso è formato dagli osteoblasti che originano da cellule mesenchimali indifferenziate. Si tratta di cellule mononucleate coinvolte nella sintesi dei componenti della matrice ossea organica. Sono localizzate in un monostrato sulla superficie ossea e sono a stretto contatto con l'osteoide. Gli osteoblasti sono responsabili della deposizione dell'osteoide e della sua successiva mineralizzazione. Il prodotto della loro attività vitale è la fosfatasi alcalina, il cui contenuto nel sangue è un indicatore indiretto della loro attività. Circondati dall'osteoide mineralizzato, alcuni osteoblasti si trasformano in osteociti, cellule mononucleate il cui citoplasma forma canali associati ai canali degli osteociti vicini. Non partecipano al rimodellamento osseo, ma sono coinvolti nel processo di distruzione perilacunare, importante per la rapida regolazione dei livelli di calcio nel siero. Il riassorbimento osseo è effettuato dagli osteoclasti, cellule polinucleate giganti, apparentemente formate dalla fusione di macrofagi mononucleati. Si presume inoltre che i precursori degli osteoclasti possano essere cellule staminali emopoietiche del midollo osseo. Sono mobili e formano uno strato a contatto con l'osso, localizzato nelle aree di maggiore riassorbimento. A causa del rilascio di enzimi proteolitici e fosfatasi acida, gli osteoclasti causano la degradazione del collagene, la distruzione dell'idrossiapatite e la rimozione di minerali dalla matrice. Il tessuto osseo scarsamente mineralizzato di nuova formazione (osteoide) è resistente al riassorbimento osteoclastico. Le funzioni degli osteoblasti e degli osteoclasti sono indipendenti, ma coordinate tra loro, il che porta a un normale rimodellamento scheletrico. La crescita ossea in lunghezza dipende dall'ossificazione encondrale, la crescita in larghezza e spessore dall'ossificazione periostale. Studi clinici con 47 Ca hanno dimostrato che fino al 18% del contenuto totale di calcio nello scheletro viene rinnovato ogni anno. Quando le ossa sono danneggiate (fratture, processi infettivi), l'osso alterato viene riassorbito e si forma nuovo osso.
I complessi cellulari coinvolti nel processo locale di riassorbimento e formazione ossea sono chiamati unità di rimodellamento multicellulare di base (BMU). Regolano la concentrazione locale di calcio, fosforo e altri ioni, la sintesi dei componenti organici dell'osso, in particolare il collagene, la sua organizzazione e mineralizzazione.
L'effetto principale dell'ormone paratiroideo nelle ossa dello scheletro è quello di migliorare i processi di riassorbimento, influenzando sia i componenti minerali che quelli organici della struttura ossea. L'ormone paratiroideo promuove la crescita degli osteoclasti e la loro attività, che si accompagna a un potenziamento dell'effetto osteolitico e a un aumento del riassorbimento osseo. In questo caso, i cristalli di idrossiapatite si dissolvono con il rilascio di calcio e fosforo nel sangue. Questo processo è il meccanismo principale per aumentare i livelli di calcio nel sangue. Consiste in tre componenti: mobilizzazione del calcio dall'osso perilacunare (osteociti profondi); proliferazione delle cellule osteoprogeneratrici in osteoclasti; mantenimento di un livello costante di calcio nel sangue regolandone il rilascio dall'osso (osteociti superficiali).
Pertanto, l'ormone paratiroideo inizialmente aumenta l'attività di osteociti e osteoclasti, favorendo l'osteolisi, causando un aumento del livello di calcio nel sangue e una maggiore escrezione di calcio e ossiprolina nelle urine. Questo è il primo effetto rapido e qualitativo dell'ormone paratiroideo. Il secondo effetto dell'ormone paratiroideo sulle ossa è quantitativo. È associato a un aumento del pool di osteoclasti. Con l'osteolisi attiva, si verifica uno stimolo per una maggiore proliferazione degli osteoblasti, attivando sia il riassorbimento che la formazione ossea con una predominanza del riassorbimento. Con un eccesso di ormone paratiroideo, si verifica un bilancio osseo negativo. Questo è accompagnato da un'eccessiva escrezione di ossiprolina, un prodotto della degradazione del collagene e di acidi sialici inclusi nella struttura dei mucopolisaccaridi. L'ormone paratiroideo attiva l'adenosina monofosfato ciclico (cAMP). L'aumentata escrezione di cAMP nelle urine dopo la somministrazione di ormone paratiroideo può fungere da indicatore di sensibilità tissutale ad esso.
L'effetto più importante del paratormone sui reni è la sua capacità di ridurre il riassorbimento del fosforo, aumentando la fosfaturia. Il meccanismo di riduzione nelle diverse parti del nefrone è diverso: nella parte prossimale, questo effetto del paratormone è dovuto all'aumento della permeabilità e si verifica con la partecipazione dell'AMP ciclico, mentre nella parte distale non dipende dal cAMP. L'effetto fosfaturico del paratormone varia in caso di carenza di vitamina D, acidosi metabolica e riduzione del contenuto di fosforo. Il paratormone aumenta leggermente il riassorbimento tubulare totale del calcio. Allo stesso tempo, lo diminuisce nelle parti prossimali e lo aumenta in quelle distali. Quest'ultimo aspetto è di fondamentale importanza: il paratormone riduce la clearance del calcio. Il paratormone riduce il riassorbimento tubulare del sodio e del suo bicarbonato, il che potrebbe spiegare lo sviluppo di acidosi nell'iperparatiroidismo. Aumenta la formazione di 1,25-diossicolecalciferolo 1,25(OH2 ) D3 nei reni, la forma attiva della vitamina D3 . Questo composto aumenta il riassorbimento del calcio nell'intestino tenue stimolando l'attività di una specifica proteina legante il calcio (CaBP) nella sua parete.
Il livello normale di ormone paratiroideo è in media 0,15-0,6 ng/ml. Varia a seconda dell'età e del sesso. Il contenuto medio di ormone paratiroideo nel sangue di persone di età compresa tra 20 e 29 anni è di (0,245±0,017) ng/ml, di 80-89 anni di (0,545±0,048) ng/ml; il livello di ormone paratiroideo nelle donne di 70 anni è di (0,728±0,051) ng/ml, e negli uomini della stessa età di (0,466±0,40) ng/ml. Pertanto, il contenuto di ormone paratiroideo aumenta con l'età, ma in misura maggiore nelle donne.
Di norma, per la diagnosi differenziale dell'ipercalcemia si dovrebbero utilizzare più test diversi.
Presentiamo la classificazione clinica e patogenetica da noi elaborata, basata sulla classificazione di OV Nikolaev e VN Tarkaeva (1974).
Classificazione clinica e patogenetica delle malattie associate a secrezione alterata dell'ormone paratiroideo e sensibilità ad esso
Iperparatiroidismo primario
- Per patogenesi:
- adenoma(i) iperfunzionante(i);
- iperplasia dell'OGD;
- carcinoma paratiroideo iperfunzionante;
- neoplasia endocrina multipla di tipo I con iperparatiroidismo (sindrome di Wermer);
- neoplasia endocrina multipla di tipo II con iperparatiroidismo (sindrome di Sipple).
- In base alle caratteristiche cliniche:
- forma dell'osso:
- osteoporotico,
- osteite fibrocistica,
- "Pagetoide";
- forma visceropatica:
- con danni predominanti a carico dei reni, del tratto gastrointestinale, della sfera neuropsichiatrica;
- forma mista.
- forma dell'osso:
- A valle:
- speziato;
- cronico.
Iperparatiroidismo secondario (iperfunzione e iperplasia secondaria delle ghiandole paratiroidi con ipocalcemia e iperfosfatemia prolungate)
- Patologia renale:
- insufficienza renale cronica;
- tubulopatia (tipo Albright-Fanconi);
- rachitismo renale.
- Patologia intestinale:
- sindrome da malassorbimento.
- Patologia ossea:
- osteomalacia senile;
- puerperale;
- idiopatico;
- Malattia di Paget.
- Carenza di vitamina D:
- nefropatia;
- fegato;
- carenze enzimatiche ereditarie.
- Malattie maligne: mieloma.
Iperparatiroidismo terziario
- Adenoma(i) autonomo(i) delle ghiandole paratiroidee, che si sviluppa su uno sfondo di iperparatiroidismo secondario di lunga durata.
Pseudoiperparatiroidismo
- Produzione dell'ormone paratiroideo da parte di tumori di origine non paratiroidea.
Formazioni cistiche e tumorali ormonalmente inattive delle ghiandole paratiroidee
- Cisti.
- Tumori o carcinomi ormonalmente inattivi.
Ipoparatiroidismo
- Sottosviluppo congenito o assenza delle ghiandole paratiroidi.
- Di origine idiopatica e autoimmune.
- Postoperatorio, sviluppato in concomitanza con la rimozione delle paratiroidi.
- Postoperatorio a causa di alterazione dell'afflusso sanguigno e dell'innervazione.
- Danni da radiazioni, esogeni ed endogeni (radioterapia a fasci esterni, trattamento delle patologie della tiroide con iodio radioattivo).
- Danni alle ghiandole paratiroidi dovuti a emorragia o infarto.
- Lesioni infettive.
Pseudoipoparatiroidismo
- Tipo I - insensibilità degli organi bersaglio all'ormone paratiroideo, dipendente dall'adenilato ciclasi;
- Tipo II - insensibilità degli organi bersaglio all'ormone paratiroideo, indipendente dall'adenilato ciclasi, probabilmente di origine autoimmune.
Pseudopseudoipoparatiroidismo
Presenza di segni somatici di pseudoipoparatiroidismo nei parenti sani delle famiglie dei pazienti con pseudoipoparatiroidismo senza disturbi biochimici caratteristici e senza tetania.
 [ 13 ], [ 14 ], [ 15 ], [ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ], [ 21 ]
[ 13 ], [ 14 ], [ 15 ], [ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ], [ 21 ]
