Esperto medico dell'articolo
Nuove pubblicazioni
Sintesi, secrezione e metabolismo delle catecolamine
Ultima recensione: 06.07.2025

Tutti i contenuti di iLive sono revisionati o verificati da un punto di vista medico per garantire la massima precisione possibile.
Abbiamo linee guida rigorose in materia di sourcing e colleghiamo solo a siti di media affidabili, istituti di ricerca accademici e, ove possibile, studi rivisti dal punto di vista medico. Nota che i numeri tra parentesi ([1], [2], ecc.) Sono link cliccabili per questi studi.
Se ritieni che uno qualsiasi dei nostri contenuti sia impreciso, scaduto o comunque discutibile, selezionalo e premi Ctrl + Invio.
La midollare del surrene produce composti con una struttura ben lontana da quella degli steroidi. Contengono un nucleo 3,4-diidrossifenile (catecolo) e sono chiamati catecolamine. Tra queste, adrenalina, noradrenalina e dopamina beta-idrossitiramina.
La sequenza della sintesi delle catecolamine è piuttosto semplice: tirosina → diidrossifenilalanina (DOPA) → dopamina → noradrenalina → adrenalina. La tirosina entra nell'organismo con il cibo, ma può anche essere formata dalla fenilalanina nel fegato sotto l'azione della fenilalanina idrossilasi. I prodotti finali della conversione della tirosina nei tessuti sono diversi. Nella midollare del surrene, il processo procede fino alla fase di formazione dell'adrenalina, nelle terminazioni dei nervi simpatici alla noradrenalina, e in alcuni neuroni del sistema nervoso centrale, la sintesi delle catecolamine termina con la formazione di dopamina.
La conversione della tirosina in DOPA è catalizzata dalla tirosina idrossilasi, i cui cofattori sono la tetraidrobiopterina e l'ossigeno. Si ritiene che questo enzima limiti la velocità dell'intero processo di biosintesi delle catecolamine e sia inibito dai prodotti finali del processo. La tirosina idrossilasi è il principale bersaglio degli effetti regolatori sulla biosintesi delle catecolamine.
La conversione della DOPA in dopamina è catalizzata dall'enzima DOPA decarbossilasi (cofattore - piridossal fosfato), che è relativamente aspecifico e decarbossila altri L-amminoacidi aromatici. Tuttavia, ci sono indicazioni della possibilità di modificare la sintesi delle catecolamine modificando l'attività di questo enzima. Alcuni neuroni sono privi di enzimi per l'ulteriore conversione della dopamina, che è il prodotto finale. Altri tessuti contengono la dopamina beta-idrossilasi (cofattori - rame, acido ascorbico e ossigeno), che converte la dopamina in noradrenalina. Nella midollare del surrene (ma non nelle terminazioni dei nervi simpatici) è presente la feniletanolammina, una metiltransferasi che forma adrenalina dalla noradrenalina. In questo caso, la S-adenosilmetionina funge da donatore di gruppi metilici.
È importante ricordare che la sintesi di feniletanolammina-N-metiltransferasi è indotta dai glucocorticoidi che entrano nella midollare dalla corteccia attraverso il sistema venoso portale. Questo potrebbe spiegare il fatto che due diverse ghiandole endocrine siano combinate in un unico organo. L'importanza dei glucocorticoidi per la sintesi di adrenalina è sottolineata dal fatto che le cellule della midollare del surrene che producono noradrenalina si trovano attorno ai vasi arteriosi, mentre le cellule che producono adrenalina ricevono sangue principalmente dai seni venosi situati nella corteccia surrenale.
La degradazione delle catecolamine avviene principalmente sotto l'influenza di due sistemi enzimatici: la catecol-O-metiltransferasi (COMT) e la monoamino ossidasi (MAO). Le principali vie di degradazione di adrenalina e noradrenalina sono illustrate schematicamente in Figura 54. Sotto l'influenza della COMT in presenza del donatore del gruppo metilico S-adrenosilmetionina, le catecolamine vengono convertite in normetanefrina e metanefrina (derivati 3-O-metilici di noradrenalina e adrenalina), che, sotto l'influenza della MAO, vengono convertite in aldeidi e quindi (in presenza di aldeide ossidasi) in acido vanilmandelico (VMA), il principale prodotto di degradazione di noradrenalina e adrenalina. Nello stesso caso, quando le catecolamine sono inizialmente esposte alle MAO anziché alla COMT, vengono convertite in aldeide 3,4-diossomandelica e poi, sotto l'influenza dell'aldeide ossidasi e della COMT, in acido 3,4-diossomandelico e VMC. In presenza di alcol deidrogenasi, il 3-metossi-4-ossifenilglicole, che è il principale prodotto finale della degradazione di adrenalina e noradrenalina nel SNC, può essere formato dalle catecolamine.
La scomposizione della dopamina è simile, fatta eccezione per il fatto che i suoi metaboliti sono privi del gruppo ossidrilico sull'atomo di carbonio beta e, pertanto, invece dell'acido vanilmandelico, si forma l'acido omovanillico (HVA) o acido 3-metossi-4-idrossifenilacetico.
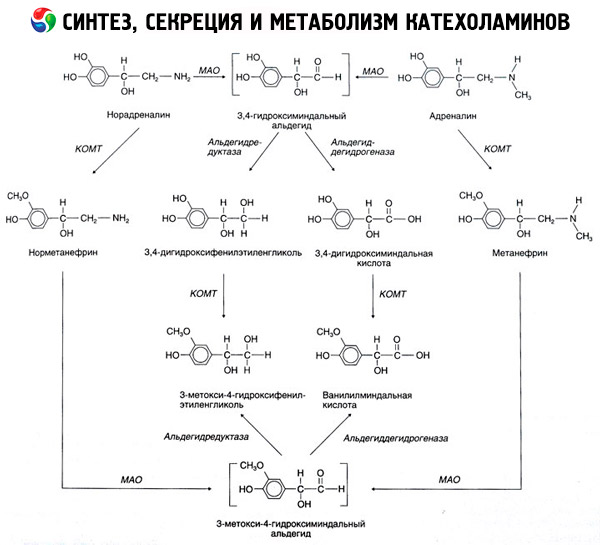
Si postula anche l'esistenza di un percorso chinoide di ossidazione della molecola di catecolamina, che può dare origine a prodotti intermedi con spiccata attività biologica.
Noradrenalina e adrenalina, prodotte sotto l'azione di enzimi citosolici nelle terminazioni nervose simpatiche e nella midollare del surrene, entrano nei granuli secretori, che li proteggono dall'azione degli enzimi di degradazione. La cattura delle catecolamine da parte dei granuli richiede un dispendio energetico. Nei granuli cromaffini della midollare del surrene, le catecolamine sono strettamente legate all'ATP (in un rapporto di 4:1) e a proteine specifiche, le cromogranine, che impediscono la diffusione degli ormoni dai granuli al citoplasma.
Lo stimolo diretto per la secrezione di catecolamine è apparentemente la penetrazione del calcio nella cellula, che stimola l'esocitosi (fusione della membrana dei granuli con la superficie cellulare e loro rottura con liberazione completa dei contenuti solubili - catecolamine, dopamina beta-idrossilasi, ATP e cromogranine - nel liquido extracellulare).
Effetti fisiologici delle catecolamine e loro meccanismo d'azione
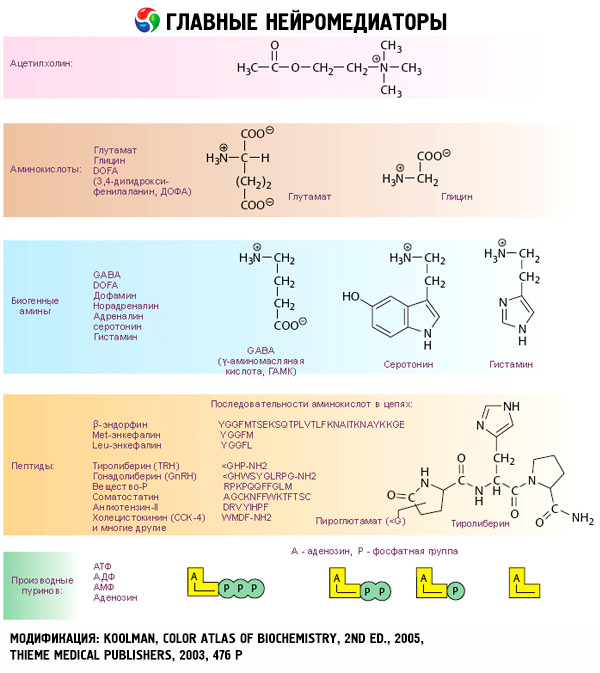
Gli effetti delle catecolamine iniziano con l'interazione con specifici recettori delle cellule bersaglio. Mentre i recettori per gli ormoni tiroidei e steroidei sono localizzati all'interno delle cellule, i recettori per le catecolamine (così come per l'acetilcolina e gli ormoni peptidici) sono presenti sulla superficie cellulare esterna.
È stato a lungo dimostrato che, in relazione ad alcune reazioni, l'adrenalina o la noradrenalina sono più efficaci della catecolamina sintetica isoproterenolo, mentre in relazione ad altre, l'effetto dell'isoproterenolo è superiore all'azione dell'adrenalina o della noradrenalina. Su questa base, è stato sviluppato il concetto della presenza di due tipi di adrenorecettori nei tessuti: alfa e beta, e in alcuni di essi può essere presente solo uno di questi due tipi. L'isoproterenolo è l'agonista più potente dei beta-adrenorecettori, mentre il composto sintetico fenilefrina è l'agonista più potente degli alfa-adrenorecettori. Le catecolamine naturali – adrenalina e noradrenalina – sono in grado di interagire con i recettori di entrambi i tipi, ma l'adrenalina mostra una maggiore affinità per i beta- e la noradrenalina per gli alfa-.
Le catecolamine attivano i recettori beta-adrenergici cardiaci più fortemente rispetto ai recettori beta della muscolatura liscia, il che ha permesso di suddividere il tipo beta in sottotipi: recettori beta1 (cuore, cellule adipose) e recettori beta2 (bronchi, vasi sanguigni, ecc.). L'effetto dell'isoproterenolo sui recettori beta1 supera quello di adrenalina e noradrenalina solo di 10 volte, mentre sui recettori beta2 agisce da 100 a 1000 volte più intensamente delle catecolamine naturali.
L'uso di antagonisti specifici (fentolamina e fenossibenzamina per i recettori alfa e propranololo per quelli beta) ha confermato l'adeguatezza della classificazione degli adrenorecettori. La dopamina è in grado di interagire sia con i recettori alfa che beta, ma vari tessuti (cervello, ipofisi, vasi) possiedono anche i propri recettori dopaminergici, il cui bloccante specifico è l'aloperidolo. Il numero di recettori beta varia da 1000 a 2000 per cellula. Gli effetti biologici delle catecolamine mediati dai recettori beta sono solitamente associati all'attivazione dell'adenilato ciclasi e a un aumento del contenuto intracellulare di cAMP. Sebbene il recettore e l'enzima siano funzionalmente collegati, si tratta di macromolecole diverse. La guanosina trifosfato (GTP) e altri nucleotidi purinici partecipano alla modulazione dell'attività dell'adenilato ciclasi sotto l'influenza del complesso ormone-recettore. Aumentando l'attività enzimatica, sembrano ridurre l'affinità dei recettori beta per gli agonisti.
Il fenomeno dell'aumentata sensibilità delle strutture denervate è noto da tempo. Al contrario, l'esposizione prolungata agli agonisti riduce la sensibilità dei tessuti bersaglio. Lo studio dei recettori beta ha permesso di spiegare questi fenomeni. È stato dimostrato che l'esposizione prolungata all'isoproterenolo porta a una perdita di sensibilità dell'adenilato ciclasi dovuta a una diminuzione del numero di recettori beta.
Il processo di desensibilizzazione non richiede l'attivazione della sintesi proteica ed è probabilmente dovuto alla graduale formazione di complessi ormone-recettore irreversibili. Al contrario, l'introduzione di 6-ossidopamina, che distrugge le terminazioni simpatiche, è accompagnata da un aumento del numero di recettori beta reattivi nei tessuti. È possibile che un aumento dell'attività nervosa simpatica causi anche una desensibilizzazione legata all'età dei vasi sanguigni e del tessuto adiposo nei confronti delle catecolamine.
Il numero di adrenorecettori in diversi organi può essere controllato da altri ormoni. Pertanto, l'estradiolo aumenta e il progesterone diminuisce il numero di alfa-adrenorecettori nell'utero, il che si accompagna a un corrispondente aumento e diminuzione della sua risposta contrattile alle catecolamine. Se il "secondo messaggero" intracellulare formato dall'azione degli agonisti dei recettori beta è certamente l'AMPc, la situazione relativa al trasmettitore degli effetti alfa-adrenergici è più complicata. Si ipotizza l'esistenza di vari meccanismi: una diminuzione del livello di AMPc, un aumento del contenuto di AMPc, la modulazione della dinamica del calcio cellulare, ecc.
Per riprodurre vari effetti nell'organismo, sono solitamente necessarie dosi di adrenalina 5-10 volte inferiori a quelle della noradrenalina. Sebbene quest'ultima sia più efficace in relazione agli α- e β-adrenorecettori, è importante ricordare che entrambe le catecolamine endogene sono in grado di interagire sia con i recettori α che β-. Pertanto, la risposta biologica di un dato organo all'attivazione adrenergica dipende in larga misura dal tipo di recettori in esso presenti. Tuttavia, ciò non significa che l'attivazione selettiva del collegamento nervoso o umorale del sistema simpatico-surrenale sia impossibile. Nella maggior parte dei casi, si osserva un aumento dell'attività dei suoi vari collegamenti. Pertanto, è generalmente accettato che l'ipoglicemia attivi in modo riflesso la midollare del surrene, mentre una diminuzione della pressione sanguigna (ipotensione posturale) è accompagnata principalmente dal rilascio di noradrenalina dalle terminazioni nervose simpatiche.
Gli adrenorecettori e gli effetti della loro attivazione in vari tessuti
Sistema, organo |
Tipo di recettore adrenergico |
Reazione |
Sistema cardiovascolare: |
||
Cuore |
Beta |
Aumento della frequenza cardiaca, della conduttività e della contrattilità |
Arteriole: |
||
Pelle e mucose |
Alfa |
Riduzione |
Muscoli scheletrici |
Beta |
Espansione Contrazione |
Organi addominali |
Alpha (altro) |
Riduzione |
Beta |
Estensione |
|
Vene |
Alfa |
Riduzione |
Apparato respiratorio: |
||
Muscoli dei bronchi |
Beta |
Estensione |
Sistema digerente: |
||
Stomaco |
Beta |
Diminuzione delle capacità motorie |
Intestini |
Alfa |
Contrazione degli sfinteri |
Milza |
Alfa |
Riduzione |
Beta |
Relax |
|
Pancreas esocrino |
Alfa |
Diminuzione della secrezione |
Sistema urogenitale: |
Alfa |
Contrazione dello sfintere |
Vescia |
Beta |
Rilassamento del muscolo eiettore |
Genitali maschili |
Alfa |
Eiaculazione |
Occhi |
Alfa |
Dilatazione della pupilla |
Pelle |
Alfa |
Aumento della sudorazione |
Ghiandole salivari |
Alfa |
Escrezione di potassio e acqua |
Beta |
Secrezione di amilasi |
|
Ghiandole endocrine: |
||
Isole del pancreas |
||
Cellule beta |
Alpha (altro) |
Diminuzione della secrezione di insulina |
Beta |
Aumento della secrezione di insulina |
|
Cellule alfa |
Beta |
Aumento della secrezione di glucagone |
8 celle |
Beta |
Aumento della secrezione di somatostatina |
Ipotalamo e ghiandola pituitaria: |
||
Somatotrofi |
Alfa |
Aumento della secrezione di STH |
Beta |
Diminuzione della secrezione di STH |
|
Lattotrofi |
Alfa |
Diminuzione della secrezione di prolattina |
Tireotrofi |
Alfa |
Diminuzione della secrezione di TSH |
Corticotrofi |
Alfa |
Aumento della secrezione di ACTH |
| beta | Diminuzione della secrezione di ACTH | |
Tiroide: |
||
Cellule follicolari |
Alfa |
Diminuzione della secrezione di tiroxina |
Beta |
Aumento della secrezione di tiroxina |
|
Cellule parafollicolari (K) |
Beta |
Aumento della secrezione di calcitonina |
Ghiandole paratiroidi |
Beta |
Aumento della secrezione di PTH |
Reni |
Beta |
Aumento della secrezione di renina |
Stomaco |
Beta |
Aumento della secrezione di gastrina |
BX |
Beta |
Aumento del consumo di ossigeno |
Fegato |
? |
Aumento della glicogenolisi e della gluconeogenesi con rilascio di glucosio; aumento della chetogenesi con rilascio di corpi chetonici |
Tessuto adiposo |
Beta |
Aumento della lipolisi con rilascio di acidi grassi liberi e glicerolo |
Muscoli scheletrici |
Beta |
Aumento della glicolisi con rilascio di piruvato e lattato; diminuzione della proteolisi con diminuzione del rilascio di alanina, glutammina |
È importante tenere presente che i risultati della somministrazione endovenosa di catecolamine non sempre riflettono adeguatamente gli effetti dei composti endogeni. Questo vale principalmente per la noradrenalina, poiché nell'organismo viene rilasciata principalmente non nel sangue, ma direttamente nelle fessure sinaptiche. Pertanto, la noradrenalina endogena attiva, ad esempio, non solo i recettori alfa vascolari (aumento della pressione sanguigna), ma anche i recettori beta cardiaci (aumento della frequenza cardiaca), mentre l'introduzione di noradrenalina dall'esterno porta principalmente all'attivazione dei recettori alfa vascolari e a un rallentamento riflesso (attraverso il nervo vago) della frequenza cardiaca.
Basse dosi di adrenalina attivano principalmente i recettori beta dei vasi muscolari e del cuore, con conseguente riduzione della resistenza vascolare periferica e aumento della gittata cardiaca. In alcuni casi, può prevalere il primo effetto e si sviluppa ipotensione dopo la somministrazione di adrenalina. A dosi più elevate, l'adrenalina attiva anche i recettori alfa, con conseguente aumento della resistenza vascolare periferica e, a fronte di un aumento della gittata cardiaca, un aumento della pressione arteriosa. Tuttavia, il suo effetto sui recettori beta vascolari viene mantenuto. Di conseguenza, l'aumento della pressione sistolica supera l'analogo indicatore della pressione diastolica (aumento della pressione differenziale). Con l'introduzione di dosi ancora più elevate, gli effetti alfa-mimetici dell'adrenalina iniziano a prevalere: la pressione sistolica e diastolica aumentano parallelamente, come sotto l'influenza della noradrenalina.
L'effetto delle catecolamine sul metabolismo consiste nei loro effetti diretti e indiretti. I primi si realizzano principalmente attraverso i recettori beta. Processi più complessi sono associati al fegato. Sebbene l'aumento della glicogenolisi epatica sia tradizionalmente considerato il risultato dell'attivazione dei recettori beta, esistono anche prove del coinvolgimento dei recettori alfa. Gli effetti indiretti delle catecolamine sono associati alla modulazione della secrezione di molti altri ormoni, come l'insulina. Nell'effetto dell'adrenalina sulla sua secrezione, la componente alfa-adrenergica predomina nettamente, poiché è stato dimostrato che qualsiasi stress è accompagnato dall'inibizione della secrezione di insulina.
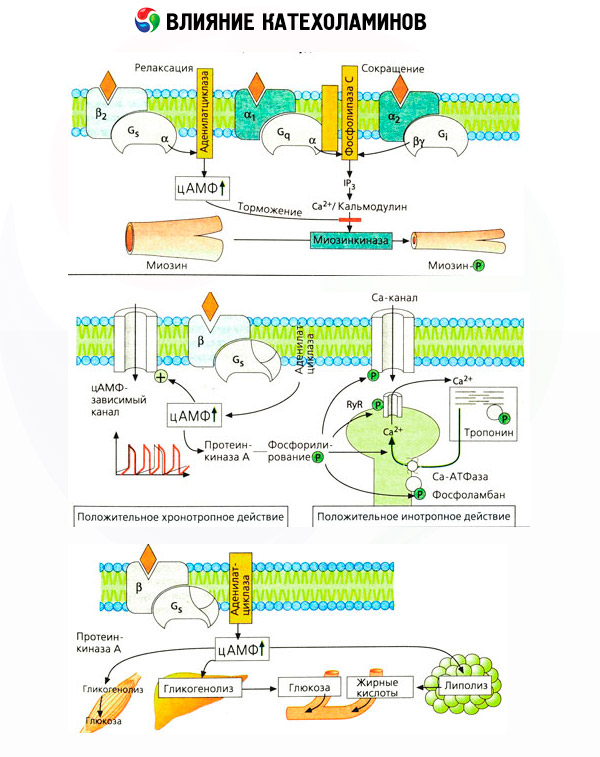
La combinazione degli effetti diretti e indiretti delle catecolamine causa iperglicemia, associata non solo all'aumento della produzione epatica di glucosio, ma anche all'inibizione del suo utilizzo da parte dei tessuti periferici. L'accelerazione della lipolisi causa iperlipacidemia con un aumento del trasporto di acidi grassi al fegato e un'intensificazione della produzione di corpi chetonici. L'aumento della glicolisi nei muscoli porta a un aumento del rilascio di lattato e piruvato nel sangue, che, insieme al glicerolo rilasciato dal tessuto adiposo, fungono da precursori della gluconeogenesi epatica.
Regolazione della secrezione di catecolamine. La similarità dei prodotti e dei metodi di reazione del sistema nervoso simpatico e della midollare surrenale ha costituito la base per la combinazione di queste strutture in un unico sistema simpatico-surrenale corporeo, con la distribuzione dei suoi collegamenti nervosi e ormonali. Vari segnali afferenti sono concentrati nell'ipotalamo e nei centri del midollo spinale e del midollo allungato, da dove hanno origine i messaggi efferenti, che si dirigono ai corpi cellulari dei neuroni pregangliari situati nelle corna laterali del midollo spinale a livello dei segmenti VIII cervicale - II-III lombare.
Gli assoni pregangliari di queste cellule lasciano il midollo spinale e formano connessioni sinaptiche con i neuroni situati nei gangli della catena simpatica o con le cellule della midollare del surrene. Queste fibre pregangliari sono colinergiche. La prima differenza fondamentale tra i neuroni postganglionari simpatici e le cellule cromaffini della midollare del surrene è che queste ultime trasmettono il segnale colinergico da loro ricevuto non per conduzione nervosa (nervi adrenergici postganglionari), ma per via umorale, rilasciando composti adrenergici nel sangue. La seconda differenza è che i nervi postganglionari producono noradrenalina, mentre le cellule della midollare del surrene producono principalmente adrenalina. Queste due sostanze hanno effetti diversi sui tessuti.

