Esperto medico dell'articolo
Nuove pubblicazioni
Cause e patogenesi dell'adenoma prostatico
Last reviewed: 04.07.2025

Tutti i contenuti di iLive sono revisionati o verificati da un punto di vista medico per garantire la massima precisione possibile.
Abbiamo linee guida rigorose in materia di sourcing e colleghiamo solo a siti di media affidabili, istituti di ricerca accademici e, ove possibile, studi rivisti dal punto di vista medico. Nota che i numeri tra parentesi ([1], [2], ecc.) Sono link cliccabili per questi studi.
Se ritieni che uno qualsiasi dei nostri contenuti sia impreciso, scaduto o comunque discutibile, selezionalo e premi Ctrl + Invio.
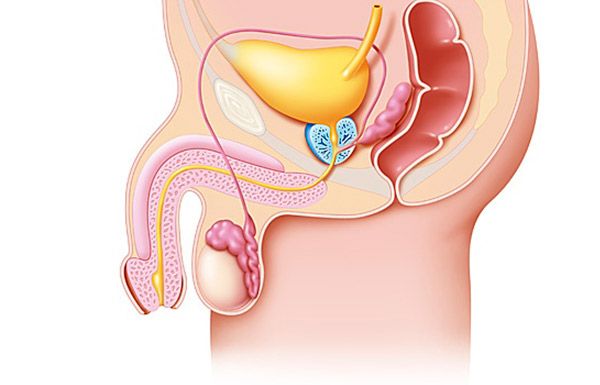
Comprendere la patogenesi dell'adenoma prostatico (ghiandola prostatica) è impossibile senza considerare i dati moderni sulla sua anatomia e morfologia. La moderna teoria dello sviluppo dell'adenoma prostatico (ghiandola prostatica) si basa sul concetto zonale della struttura prostatica, secondo il quale si distinguono diverse aree nella ghiandola prostatica, che differiscono per le caratteristiche istologiche e funzionali degli elementi cellulari che le compongono. Queste sono le zone periferica, centrale e di transizione (transitoria), nonché l'area dello stroma fibromuscolare anteriore e il segmento preprostatico.
Nella zona del tubercolo seminale si aprono le aperture di deflusso dei vasi deferenti. La parete della parte prossimale dell'uretra è costituita da fibre muscolari lisce longitudinali. Lo sfintere preprostatico (genitale), formato da uno spesso strato di fibre muscolari lisce, circonda la parte prossimale dell'uretra dal collo vescicale alla sommità del tubercolo seminale e impedisce l'eiaculazione retrograda.
Studi istologici hanno dimostrato che la crescita dell'adenoma prostatico (ghiandola prostatica) inizia nelle zone centrale e di transizione della prostata. La zona di transizione della prostata è costituita da due ghiandole separate situate immediatamente dietro lo sfintere interno della vescica. I dotti escretori di questa zona si trovano sulla parete laterale dell'uretra, vicino al tubercolo seminale. La zona di transizione prossimale contiene le ghiandole della zona periuretrale, che confinano con lo sfintere interno della vescica e sono situate parallelamente all'asse dell'uretra. I linfonodi adenomatosi possono svilupparsi sia nella zona di transizione che nella zona parauretrale. Oltre all'iperplasia nodulare, la zona di transizione tende a crescere con l'età.
La capsula prostatica svolge un ruolo importante nello sviluppo dei sintomi dell'adenoma prostatico (ghiandola prostatica). Pertanto, nei cani, la capsula prostatica è poco sviluppata e, anche in caso di iperplasia pronunciata, i sintomi della malattia si manifestano raramente. La capsula trasmette la pressione del tessuto prostatico ingrossato all'uretra, causando un aumento della resistenza uretrale.
Adenoma prostatico (ghiandola prostatica): fisiopatologia
La parte prostatica dell'uretra si allunga e si deforma fino a 4-6 cm o più, principalmente a causa dell'area della parete posteriore situata al di sopra del tubercolo seminale. Il collo vescicale si solleva e si deforma, il suo lume assume la forma di una fessura. Di conseguenza, la curvatura naturale dell'uretra aumenta e, con lo sviluppo irregolare dei lobi laterali, l'uretra si curva anche in direzione trasversale, assumendo un aspetto a zigzag. L'apertura del lume del collo vescicale, dovuta al fallimento del meccanismo uretro-sfinteriale durante la compensazione detrusoriale, si manifesta clinicamente con l'incontinenza urinaria.
Anche la vescica urinaria subisce profondi cambiamenti. La sua reazione allo sviluppo dell'ostruzione attraversa tre fasi: irritabilità, compensazione e scompenso. Nella prima fase dell'ostruzione infravescicale, la vescica urinaria risponde aumentando le contrazioni detrusoriali, consentendo il temporaneo mantenimento dell'equilibrio funzionale e la completa evacuazione dell'urina. Un ulteriore sviluppo dell'ostruzione porta a un'ipertrofia compensatoria della parete vescicale, che può raggiungere i 2-3 cm di spessore. In questo caso, può acquisire un aspetto trabecolare a causa dell'ispessimento e della protrusione dei fasci muscolari.
Lo stadio iniziale dello sviluppo trabecolare è morfologicamente caratterizzato dall'ipertrofia delle cellule muscolari lisce. La progressione del processo porta alla separazione degli elementi muscolari ipertrofici e al riempimento degli spazi tra di essi con tessuto connettivo. Tra le trabecole si formano depressioni chiamate falsi diverticoli, le cui pareti si assottigliano gradualmente a causa dell'aumentata pressione intravescicale. Tali diverticoli sono spesso multipli, raggiungendo talvolta dimensioni significative.
Le proprietà elastiche del detrusore sono determinate dalla presenza di collagene, che nel suo tessuto muscolare liscio costituisce il 52% della quantità totale di proteine. Con l'esaurimento delle capacità compensatorie e l'aumento dell'atrofia, le pareti della vescica si assottigliano. Il detrusore perde la sua capacità di contrarsi e allungarsi, con conseguente aumento della capacità della vescica, che raggiunge 1 litro o più. Le alterazioni infiammatorie e trofiche concomitanti portano a una marcata sclerosi dello strato muscolare della parete vescicale e a una diminuzione del contenuto di collagene. Il contenuto di tessuto connettivo diventa uguale o superiore a quello degli elementi muscolari.
Il grado di ripristino della normale struttura della parete vescicale dipende dalla durata dell'ostruzione al deflusso urinario. A seguito di un'ostruzione prolungata, si sviluppano alterazioni morfologiche irreversibili che portano a gravi disturbi funzionali della vescica, ineliminabili anche con un intervento chirurgico. Un'ostruzione infravescicale grave comporta un aumento della pressione vescicale, una compromissione del deflusso urinario dai reni e lo sviluppo di reflusso vescico-ureterale e renale, nonché pielonefrite. Gli ureteri si dilatano, si allungano, diventano tortuosi e si sviluppano ureteroidronefrosi e insufficienza renale cronica. La patogenesi delle alterazioni renali e delle vie urinarie superiori nei pazienti con adenoma prostatico è complessa e dipende da molti fattori: alterazioni legate all'età, patologie concomitanti che ne compromettono la capacità funzionale, sviluppo di uropatia ostruttiva.
Nella prima fase dell'uropatia ostruttiva, la conservazione dell'apparato fornicale dei calici e l'integrità dell'epitelio dei tubuli collettori delle papille prevengono il verificarsi di reflussi pelvici renali e la penetrazione ascendente dell'infezione nel parenchima renale. Con lo sviluppo dell'ureteroidronefrosi, si verifica una deformazione strutturale delle volte caliceali, che crea condizioni favorevoli per il verificarsi di reflussi pelvico-tubulari renali e, successivamente, di reflussi pelvico-venosi renali e pelvico-linfatici renali.
A causa dell'aumento della pressione intrapelvica e del reflusso renale-pelvi renale, l'emodinamica renale è significativamente compromessa, con conseguente sviluppo di alterazioni strutturali nelle arterie intraorgano sotto forma di obliterazione e stenosi diffusa. I disturbi emodinamici portano a gravi alterazioni metaboliche e a una grave ischemia del tessuto renale. L'uropatia ostruttiva determina un progressivo deterioramento di tutti gli indicatori dello stato funzionale dei reni. Una caratteristica di questo processo è una precoce compromissione della capacità di concentrazione renale, che si manifesta principalmente con una forte diminuzione del riassorbimento degli ioni Na e un aumento della loro escrezione urinaria. Una compromissione della funzionalità renale nell'adenoma prostatico di stadio I si osserva nel 18% dei pazienti. Nello stadio II, l'insufficienza renale cronica complica il decorso della malattia nel 74% dei casi, di cui l'11% in fase terminale. L'insufficienza renale cronica viene rilevata in tutti i pazienti con adenoma prostatico allo stadio III, mentre lo stadio intermittente è stato osservato nel 63% dei casi e quello terminale nel 25% dei casi esaminati.
L'infezione delle vie urinarie è di fondamentale importanza nella patogenesi delle patologie renali nell'adenoma prostatico e complica significativamente il decorso della malattia. Pielonefrite e insufficienza renale rappresentano fino al 40% delle cause di morte nei pazienti con adenoma prostatico. La pielonefrite cronica nei pazienti con adenoma prostatico si osserva nel 50-90% dei casi.
L'infiammazione di origine batterica si verifica principalmente nel tessuto peritubulare interstiziale. Nella patogenesi della pielonefrite secondaria nell'adenoma prostatico, il ruolo principale è svolto dall'urostasi, dallo sviluppo di reflusso vescico-ureterale e dalla pelvi renale. L'infezione penetra nel rene risalendo dalla vescica. L'infezione delle vie urinarie accompagna la maggior parte dei casi di adenoma prostatico. La cistite cronica è stata osservata nel 57-61% dei pazienti ambulatoriali e nell'85-92% dei pazienti ricoverati. A questo proposito, la patogenesi della pielonefrite cronica nei pazienti con adenoma prostatico può essere rappresentata come segue: ostruzione infravescicale → disfunzione vescicale → cistite → insufficienza delle giunzioni vescico-ureterali → reflusso vescico-ureterale → pielonefrite cronica.
La presenza di un processo infiammatorio concomitante nella prostata gioca un ruolo importante nella formazione del quadro clinico dell'adenoma prostatico. La frequenza di prostatite cronica nell'adenoma prostatico, secondo i dati di laboratorio, chirurgici e autoptici, è rispettivamente del 73, 55,5 e 70%. La stasi venosa, la compressione dei dotti escretori degli acini da parte del tessuto iperplastico della ghiandola e il suo edema sono prerequisiti per lo sviluppo di infiammazione cronica. L'esame morfologico del materiale chirurgico ha mostrato che nella maggior parte dei casi il processo infiammatorio era localizzato alla periferia della ghiandola. La prostatite cronica concomitante può manifestarsi clinicamente con disuria, che richiede una diagnosi differenziale con i disturbi della minzione causati dall'adenoma prostatico stesso. La sua presenza porta anche a un aumento del numero di complicanze postoperatorie precoci e tardive, per cui sono necessarie misure per identificare e sanificare la prostatite cronica nella fase di trattamento conservativo o di preparazione all'intervento chirurgico.
I calcoli vescicali in un adenoma si formano secondariamente a disturbi dello svuotamento vescicale. Sono rilevati nell'11,7-12,8% dei pazienti. Di solito hanno una forma rotonda regolare, possono essere singoli o multipli e, per composizione chimica, sono urati o fosfati. I calcoli renali accompagnano l'adenoma prostatico nel 3,6-6,0% dei casi.
Una complicanza comune dell'adenoma prostatico è la ritenzione urinaria acuta completa, che può svilupparsi in qualsiasi fase della malattia. In alcuni casi, questa è la fase culminante del processo ostruttivo in combinazione con lo scompenso della capacità contrattile del detrusore, mentre in altri si sviluppa improvvisamente sullo sfondo di sintomi moderati di disturbi della minzione. Spesso, questa è la prima manifestazione clinica dell'adenoma prostatico. Secondo la letteratura, questa complicanza si osserva nel 10-50% dei pazienti, il più delle volte si verifica allo stadio II della malattia. Fattori scatenanti per lo sviluppo di questa complicanza possono essere una dieta scorretta (assunzione di alcol, spezie), ipotermia, stitichezza, svuotamento prematuro della vescica, stress, assunzione di determinati farmaci (anticolinergici, tranquillanti, antidepressivi, diuretici).
I principali fattori che determinano lo sviluppo di ritenzione urinaria acuta sono la crescita di tessuto iperplastico, alterazioni funzionali del tono del collo e della muscolatura della vescica e alterazione della microcircolazione degli organi pelvici con sviluppo di edema prostatico.
Nella fase iniziale della ritenzione urinaria acuta, l'aumentata attività contrattile del detrusore porta a un aumento della pressione intravescicale. Nelle fasi successive, a causa dello stiramento della parete vescicale e della riduzione della sua capacità contrattile, la pressione intravescicale diminuisce.

