Esperto medico dell'articolo
Nuove pubblicazioni
Cateterismo cardiaco
Ultima recensione: 06.07.2025

Tutti i contenuti di iLive sono revisionati o verificati da un punto di vista medico per garantire la massima precisione possibile.
Abbiamo linee guida rigorose in materia di sourcing e colleghiamo solo a siti di media affidabili, istituti di ricerca accademici e, ove possibile, studi rivisti dal punto di vista medico. Nota che i numeri tra parentesi ([1], [2], ecc.) Sono link cliccabili per questi studi.
Se ritieni che uno qualsiasi dei nostri contenuti sia impreciso, scaduto o comunque discutibile, selezionalo e premi Ctrl + Invio.
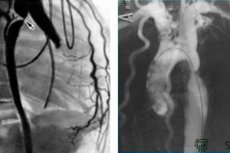
La cateterizzazione delle cavità cardiache viene eseguita mediante puntura e inserimento percutaneo di un catetere in un vaso: una vena periferica (ulnare, succlavia, giugulare, femorale) per le camere destre del cuore o un'arteria (brachiale, femorale, ascellare, radiale) per le camere sinistre del cuore.
Metodologia per l'esecuzione del cateterismo cardiaco
In caso di grave restringimento della valvola aortica o della sua protesi artificiale, quando è impossibile introdurre retrogradamente un catetere nel ventricolo sinistro, si utilizza una puntura transettale del setto interatriale dall'atrio destro a quello sinistro e quindi nel ventricolo sinistro. L'approccio più frequentemente utilizzato al vaso è secondo il metodo di Seldinger (1953). Dopo anestesia locale della cute e del tessuto sottocutaneo con soluzione di novocaina allo 0,5-1% o soluzione di lidocaina al 2% e una piccola incisione cutanea, si punge una vena o un'arteria con un ago; quando fuoriesce sangue dalla punta prossimale dell'ago (padiglione) (è necessario cercare di pungere solo la parete anteriore del vaso), si inserisce una guida attraverso l'ago, l'ago viene rimosso e un catetere viene introdotto nel vaso lungo la guida, che, naturalmente, deve essere più lunga del catetere. Il catetere viene fatto avanzare fino alla posizione desiderata sotto controllo radiografico. In caso di utilizzo di cateteri galleggianti di tipo Swan-Gans con palloncino all'estremità, la posizione della punta del catetere è determinata dalla curva di pressione. È preferibile installare un introduttore a parete sottile con valvola emostatica e un ramo laterale per il lavaggio nel vaso, attraverso il quale è facile inserire il catetere e sostituirlo con un altro se necessario. Il catetere e l'introduttore vengono lavati con soluzione isotonica di cloruro di sodio eparinizzata per prevenire la formazione di trombi. Utilizzando diversi tipi di cateteri, è possibile raggiungere diverse parti del cuore e dei vasi, misurarne la pressione, prelevare campioni di sangue per ossimetria e altri esami, introdurre la vena cava inferiore (RVC) per determinare parametri anatomici, costrizioni, perdite ematiche, ecc.
In assenza di controllo fluoroscopico (radiografico) sulla posizione del catetere, vengono utilizzati cateteri con un palloncino galleggiante gonfiabile all'estremità, che può muoversi con il flusso sanguigno nell'atrio destro, nel ventricolo destro e nell'arteria polmonare e registrarne la pressione. La pressione di incuneamento dell'arteria polmonare consente di valutare indirettamente lo stato della funzione del ventricolo sinistro, ovvero la sua pressione telediastolica (EDP), poiché l'EDP del ventricolo sinistro è la pressione media nell'atrio sinistro o la pressione nei capillari polmonari. Questo è importante per il monitoraggio della terapia in caso di ipotensione, insufficienza cardiaca, ad esempio nell'infarto miocardico acuto. Se il catetere è dotato di dispositivi aggiuntivi, è possibile misurare la gittata cardiaca mediante diluizione con colorante o termodiluizione, registrare un elettrogramma intracavitario ed eseguire la stimolazione endocardica. Le curve di pressione intracavitaria vengono registrate utilizzando un sensore di pressione del liquido Statham e un ECG su un registratore a getto o un computer con possibilità di stampa su carta; i loro cambiamenti possono essere utilizzati per valutare una particolare patologia cardiaca.
Misurazione della gittata cardiaca
È importante notare che non esistono metodi assolutamente accurati per misurare la gittata cardiaca. Durante il cateterismo cardiaco, i tre metodi più comunemente utilizzati per determinare la gittata cardiaca sono: il metodo di Fick, il metodo della termodiluizione e il metodo angiografico.
Il metodo di Fick
Fu proposto da Adolph Fick nel 1870. Il metodo si basa sul presupposto che, a riposo, l'apporto di ossigeno ai polmoni sia pari alla quantità di ossigeno utilizzata dai tessuti e che la quantità di sangue espulsa dal ventricolo sinistro sia pari al volume di sangue che scorre attraverso i polmoni. È necessario prelevare sangue venoso misto, poiché la concentrazione di ossigeno nel sangue della vena cava e del seno coronarico differisce significativamente. Il sangue viene prelevato dal ventricolo destro o dall'arteria polmonare, preferibile. La differenza di ossigeno artero-venoso può essere determinata dalla concentrazione di ossigeno nel sangue arterioso (Ca) e venoso (Cv). Calcolando il contenuto di ossigeno assorbito in 1 minuto, è possibile calcolare il volume di sangue che scorre attraverso i polmoni nello stesso periodo di tempo, ovvero la gittata cardiaca (CO):
MO = Q / Ca - St (l/min),
Dove Q è l'assorbimento di ossigeno da parte del corpo (ml/min).
Conoscendo l'indice cardiaco, è possibile calcolare l'indice cardiaco (IC). Per farlo, dividere l'indice cardiaco per la superficie del gel del paziente, calcolata in base all'altezza e al peso corporeo. L'indice cardiaco in un adulto è normalmente di 5-6 l/min e l'IC è di 2,8-3,5 l/min/ m².
Metodo di termodiluizione
Questo metodo utilizza una soluzione isotonica raffreddata di cloruro di sodio (5-10 ml), introdotta nell'atrio destro attraverso un catetere multilume; la punta del catetere con il termistore si trova nell'arteria polmonare. La calibrazione delle curve viene effettuata attivando brevemente una resistenza costante, che fornisce deviazioni del dispositivo di registrazione corrispondenti a una determinata variazione di temperatura per un dato termistore. La maggior parte dei dispositivi di termodiluizione è dotata di dispositivi di calcolo analogici. Le apparecchiature moderne consentono fino a 3 misurazioni della MO nel sangue in 1 minuto e più ripetizioni degli studi. La gittata cardiaca, o MO, è determinata dalla seguente formula: MO = V (T1 - T2) x 60 x 1,08 / S (l/min).
Dove V è il volume dell'indicatore introdotto; T1 è la temperatura del sangue; T2 è la temperatura dell'indicatore; S è l'area sotto la curva di diluizione; 1,08 è il coefficiente che dipende dalla densità specifica e dalla capacità termica del sangue e della soluzione isotonica di cloruro di sodio.
I vantaggi della termodiluizione, nonché la necessità di cateterizzare solo il letto venoso, rendono questo metodo attualmente il più accettabile per la determinazione della gittata cardiaca nella pratica clinica.
Alcuni aspetti tecnici del laboratorio di cateterizzazione
Il personale del laboratorio di angiografia con cateterismo comprende il primario, i medici, gli infermieri di sala operatoria e i tecnici di radiologia (tecnici di radiologia) se si utilizzano radiografie cine e di grande formato. Nei laboratori che utilizzano solo pellicole video e registrazione computerizzata delle immagini, i tecnici di radiologia non sono necessari. Tutto il personale di laboratorio deve essere esperto nelle tecniche di rianimazione cardiopolmonare, per le quali la sala operatoria di radiologia deve disporre dei farmaci appropriati, di un defibrillatore, di un dispositivo per la stimolazione elettrica del cuore con un set di cateteri elettrodici, di un ossigenoterapia centralizzata e (preferibilmente) di un apparecchio per la ventilazione artificiale dei polmoni.
Procedure diagnostiche complesse e rischiose e PCI (angioplastica, stenting, aterectomia, ecc.) dovrebbero essere eseguite preferibilmente in cliniche dotate di un'équipe di cardiochirurgia. Secondo le raccomandazioni dell'American College of Cardiology/American Heart Association, l'angioplastica e la visita di pazienti ad alto rischio di complicanze, come l'infarto miocardico acuto (IMA), possono essere eseguite da specialisti esperti e qualificati senza la presenza di supporto cardiochirurgico in ospedale, se il paziente non può essere trasportato in una sede più idonea senza rischi aggiuntivi. In Europa e in alcuni altri paesi (tra cui la Russia), gli interventi endovascolari vengono sempre più spesso eseguiti senza la presenza di cardiochirurghi, poiché la necessità di interventi di cardiochirurgia d'urgenza è attualmente estremamente bassa. Un accordo con una clinica di chirurgia cardiovascolare vicina è sufficiente per il trasferimento d'urgenza del paziente in caso di complicanze peri- e post-procedurali.
Per mantenere l'idoneità, la qualificazione e le competenze degli operatori, il laboratorio deve eseguire almeno 300 procedure all'anno e ogni medico deve eseguire almeno 150 procedure diagnostiche all'anno. Per la cateterizzazione e l'angiografia, sono necessari un'unità angiografica a raggi X ad alta risoluzione, un sistema per il monitoraggio dell'ECG e della pressione intravascolare, l'archiviazione e l'elaborazione delle immagini angiografiche, strumenti sterili e vari tipi di cateteri (diversi tipi di cateteri per angiografia coronarica sono descritti di seguito). L'unità angiografica deve essere dotata di un attacco per l'acquisizione e l'archiviazione di immagini cineangiografiche o digitali computerizzate, e deve essere in grado di ottenere immagini online, ovvero immediatamente con analisi computerizzata quantitativa degli angiogrammi.
Cambiamenti nelle curve di pressione intracavitaria
Le curve di pressione intracavitaria possono variare in diverse condizioni patologiche. Queste variazioni sono utili per la diagnosi quando si esaminano pazienti con diverse patologie cardiache.
Per comprendere le cause delle variazioni di pressione nelle cavità cardiache, è necessario avere un'idea delle relazioni temporali tra i processi meccanici ed elettrici che si verificano durante il ciclo cardiaco. L'ampiezza dell'onda a nell'atrio destro è maggiore dell'ampiezza dell'onda y. Un eccesso dell'onda y rispetto all'onda a nella curva di pressione dell'atrio destro indica una violazione del riempimento atriale durante la sistole ventricolare, che si verifica in caso di insufficienza o difetto della valvola tricuspide.
Nella stenosi tricuspidale, la curva di pressione atriale destra assomiglia a quella dell'atrio sinistro nella stenosi mitralica o nella pericardite costrittiva, con un declino e un plateau in diastole meso- e telediastolica, tipici delle pressioni elevate durante la sistole precoce. La pressione atriale sinistra media corrisponde abbastanza fedelmente alla pressione di incuneamento dell'arteria polmonare e alla pressione diastolica del tronco polmonare. Nell'insufficienza mitralica senza stenosi, si verifica un rapido declino della pressione all'inizio della sistole (una diminuzione dell'onda y), seguito da un graduale aumento in diastole telediastolica (diastasi). Ciò riflette il raggiungimento dell'equilibrio tra le pressioni atriale e ventricolare durante la fase tardiva del riempimento ventricolare. Al contrario, nei pazienti con stenosi mitralica, l'onda y diminuisce lentamente, mentre la pressione nell'atrio sinistro continua a diminuire per tutta la diastole, e non vi sono segni di diastasi della pressione differenziale nell'atrio sinistro, poiché il gradiente pressorio atrioventricolare è preservato. Se la stenosi mitralica è accompagnata da un ritmo sinusale normale, l'onda α nell'atrio sinistro è preservata e la contrazione degli atri determina la creazione di un ampio gradiente pressorio. Nei pazienti con insufficienza mitralica isolata, l'onda V è chiaramente espressa e presenta un ginocchio discendente ripido della linea y.
Sulla curva di pressione del ventricolo sinistro, il punto di EDP precede immediatamente l'inizio della contrazione isometrica e si trova immediatamente dopo l'onda a, prima dell'onda c della pressione atriale sinistra. L'EDP del ventricolo sinistro può aumentare nei seguenti casi: scompenso cardiaco, se il ventricolo è sottoposto a un carico elevato causato da un flusso sanguigno eccessivo, ad esempio in caso di insufficienza aortica o mitralica; ipertrofia ventricolare sinistra, accompagnata da una riduzione della sua distensibilità, elasticità e compliance; cardiomiopatia restrittiva; pericardite costrittiva; tamponamento cardiaco causato da versamento pericardico.
Nella stenosi valvolare aortica, che è accompagnata da ostruzione del deflusso sanguigno dal ventricolo sinistro e da un aumento della pressione al suo interno rispetto alla pressione sistolica nell'aorta, ovvero dalla comparsa di un gradiente di pressione, la curva di pressione del ventricolo sinistro assomiglia alla curva di pressione durante la contrazione isometrica. I suoi contorni sono più simmetrici e la pressione massima si sviluppa più tardi rispetto agli individui sani. Un quadro simile si osserva quando si registra la pressione nel ventricolo destro nei pazienti con stenosi dell'arteria polmonare. Le curve della pressione sanguigna possono anche differire nei pazienti con diversi tipi di stenosi aortica. Pertanto, nella stenosi valvolare si osserva un aumento lento e ritardato dell'onda di polso arterioso, mentre nella cardiomiopatia ipertrofica, il brusco aumento iniziale della pressione è sostituito da una rapida diminuzione e quindi da un'onda positiva secondaria che riflette l'ostruzione durante la sistole.
Indici derivati della pressione intraventricolare
La velocità di variazione/aumento della curva di pressione intraventricolare durante la fase di contrazione isovolumica è chiamata derivata prima - dр/dt. In precedenza, veniva utilizzata per valutare la contrattilità del miocardio ventricolare. Il valore di dр/dt e la derivata seconda - dр/dt/р - vengono calcolati a partire dalla curva di pressione intraventricolare utilizzando tecnologie elettroniche e informatiche. I valori massimi di questi indicatori rappresentano gli indici della frequenza di contrazione ventricolare e aiutano a valutare la contrattilità e lo stato inotropo del cuore. Purtroppo, l'ampia gamma di questi indicatori in diverse categorie di pazienti non ci consente di sviluppare standard medi, ma sono ampiamente applicabili in un singolo paziente con dati iniziali e nel contesto dell'uso di farmaci che migliorano la funzione contrattile del muscolo cardiaco.
Attualmente, disponendo di metodi di esame dei pazienti quali l'ecocardiografia nelle sue varie varianti, la TAC computerizzata, la radiografia a fascio di elettroni e la risonanza magnetica (RM), questi indicatori per la diagnosi delle patologie cardiache non sono più così importanti come in passato.
Complicanze del cateterismo cardiaco
Il cateterismo cardiaco è relativamente sicuro, tuttavia, come qualsiasi tecnica invasiva, presenta una certa percentuale di complicanze associate sia all'intervento stesso che alle condizioni generali del paziente. L'utilizzo di cateteri atraumatici più avanzati e sottili, di sistemi di ventilazione non vascolare (RVS) a bassa osmolarità e/o non ionici, e di moderne unità angiografiche con elaborazione computerizzata delle immagini in tempo reale per interventi invasivi ha ridotto significativamente l'incidenza di possibili complicanze. Pertanto, la mortalità durante il cateterismo cardiaco nei grandi laboratori angiografici non supera lo 0,1%. S. Pepine et al. riportano un tasso di mortalità complessivo fino allo 0,14%, con un'incidenza dell'1,75% per i pazienti di età inferiore a 1 anno, dello 0,25% per le persone di età superiore a 60 anni, dello 0,03% per la coronaropatia monovascolare, dello 0,16% per la coronaropatia trivascolare e dello 0,86% per la coronaropatia sinistra. In caso di insufficienza cardiaca, la mortalità aumenta anche a seconda della classe NUHA: in FC I-II - 0,02%, III e IV FC - 0,12 e 0,67%, rispettivamente. In alcuni pazienti, il rischio di gravi complicanze è aumentato. Si tratta di pazienti con angina instabile e progressiva, infarto miocardico recente (meno di 7 giorni), segni di edema polmonare dovuto a ischemia miocardica, con insufficienza circolatoria di FC III-IV, grave insufficienza ventricolare destra, difetti cardiaci valvolari (stenosi aortica grave e insufficienza aortica con una pressione differenziale superiore a 80 mm Hg), difetti cardiaci congeniti con ipertensione polmonare e insufficienza ventricolare destra.
In un'analisi multivariata di 58.332 pazienti, i fattori predittivi di complicanze gravi erano insufficienza cardiaca congestizia grave, ipertensione, cardiopatia coronarica, valvulopatia aortica e mitralica, insufficienza renale, angina instabile e infarto miocardico acuto nelle prime 24 ore, e cardiomiopatia. Nei pazienti di 80 anni, la mortalità durante le procedure diagnostiche invasive è aumentata allo 0,8% e l'incidenza di complicanze vascolari nel sito di puntura ha raggiunto il 5%.


 [
[