Esperto medico dell'articolo
Nuove pubblicazioni
Meningite criptococcica
Ultima recensione: 12.07.2025

Tutti i contenuti di iLive sono revisionati o verificati da un punto di vista medico per garantire la massima precisione possibile.
Abbiamo linee guida rigorose in materia di sourcing e colleghiamo solo a siti di media affidabili, istituti di ricerca accademici e, ove possibile, studi rivisti dal punto di vista medico. Nota che i numeri tra parentesi ([1], [2], ecc.) Sono link cliccabili per questi studi.
Se ritieni che uno qualsiasi dei nostri contenuti sia impreciso, scaduto o comunque discutibile, selezionalo e premi Ctrl + Invio.
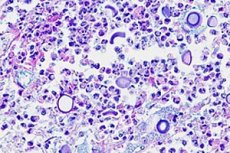
L'infiammazione delle meningi può essere causata non solo da batteri, virus e protisti, ma anche da infezioni fungine. La meningite criptococcica è causata dal fungo lievito incapsulato Cryptococcus neoformans, un agente patogeno opportunista dell'uomo. [ 1 ] È stata chiamata malattia di Busse-Buschke a causa della sua prima descrizione da parte di Otto Busse e Abraham Buschke nel 1894. [ 2 ]
Secondo l'ICD-10, il codice della malattia è G02.1 (nella sezione sulle malattie infiammatorie del sistema nervoso centrale) e anche B45.1 nella sezione sulle micosi (ovvero malattie fungine).
Epidemiologia
Otto casi su dieci di meningite criptococcica si verificano in persone infette da HIV/AIDS.
Secondo i dati pubblicati su The Lancet Infectious Diseases nella primavera del 2017, il fungo causa ogni anno circa 220.000 casi di meningite criptococcica tra le persone affette da HIV o AIDS, con oltre 180.000 decessi. La maggior parte dei casi di meningite criptococcica si verifica nell'Africa subsahariana.
Secondo le statistiche dell'OMS, nel 2017 sono stati registrati 165.800 casi di meningite criptococcica in Africa, 43.200 nei paesi asiatici, 9.700 in Nord e Sud America e 4.400 casi della stessa malattia nei paesi europei.
Le cause meningite criptococcica
Le cause di questo tipo di meningite sono l'infezione con il fungo Cryptococcus neoformans (classe Tremellomycetes, genere Filobasidiella), che vive nell'ambiente: nel terreno (inclusa la polvere), sul legno in decomposizione, negli escrementi di uccelli (piccioni) e pipistrelli, ecc. L'infezione avviene attraverso l'aria - inalando basidiospore aerosol del fungo, anche se nella maggior parte delle persone con sufficiente immunità allo sviluppo della malattia, C. neoformans non porta e rimane un microrganismo opportunista intracellulare facoltativo (che non può infettare altre persone). Leggi anche - Criptococchi - agenti causali della criptococcosi [ 3 ]
Di regola, la meningite criptococcica si sviluppa negli individui infetti da HIV (allo stadio IVB) – come infezione secondaria, nonché nelle persone con un sistema immunitario malfunzionante in altre malattie accompagnate da immunosoppressione a lungo termine. [ 4 ]
La meningite criptococcica è considerata una forma cerebrale o extrapolmonare di criptococcosi, che si sviluppa dopo la disseminazione ematogena di C. neoformans dalle vie respiratorie e dai polmoni al cervello e al midollo spinale.[ 5 ]
Fattori di rischio
I fattori che aumentano il rischio di sviluppare la meningite criptococcica includono:
- periodo neonatale (periodo neonatale) e prematurità dei neonati;
- indebolimento del sistema immunitario nelle malattie oncologiche (tra cui leucemia, melanoma multiplo, linfosarcoma), nei pazienti con infezione da HIV e AIDS;
- diabete;
- epatite virale e altre malattie immunocomplesse;
- anemia falciforme;
- chemioterapia in presenza di diagnosi oncologica;
- superamento del livello ammissibile di radiazioni ionizzanti;
- lunghi cicli di trattamento antibiotico o steroideo;
- installazione di cateteri intravascolari e shunt;
- trapianto di midollo osseo o di organi interni.
Patogenesi
I criptococchi, protetti dalle cellule immunitarie umane da una capsula polisaccaridica (che inibisce la fagocitosi), secernono proteasi, ureasi, fosfolipasi e nucleasi, enzimi capaci di distruggere le cellule ospiti. [ 6 ]
La patogenesi della criptococcosi risiede nel fatto che questi enzimi danneggiano le cellule lisando le membrane, modificando le molecole, interrompendo le funzioni degli organelli cellulari e cambiando il citoscheletro. [ 7 ]
Le serina proteasi fungine distruggono i legami peptidici delle proteine cellulari, scindono le immunoglobuline e le proteine delle cellule effettrici immunitarie e la replicazione del C. neoformans avviene all'interno dei fagociti mononucleari (macrofagi), il che ne facilita la diffusione. [ 8 ]
Inoltre, passando attraverso le cellule endoteliali e venendo trasportati all’interno dei macrofagi infetti, i criptococchi interrompono l’integrità della barriera emato-encefalica (BBB). Il fungo si diffonde attraverso il flusso sanguigno nel liquido cerebrospinale e poi nelle membrane molli del cervello, formando “colonie” di cellule fungine nel tessuto cerebrale sotto forma di pseudocisti gelatinose. [ 9 ]
Sintomi meningite criptococcica
I primi sintomi della meningite criptococcica sono febbre (la temperatura sale fino a +38,5-39 °C) e forti mal di testa.
I sintomi clinici includono anche nausea e vomito, convulsioni, rigidità del collo, aumentata sensibilità degli occhi alla luce e disturbi della coscienza e del comportamento. [ 10 ]
Come sottolineano gli esperti, lo sviluppo della sindrome meningea è più lento rispetto all'infezione batterica delle meningi.
Complicazioni e conseguenze
Le complicazioni e le conseguenze della meningite fungina causata dal Cryptococcus sono:
- aumento significativo della pressione intracranica;
- danno isolato ai nervi cranici con paresi/paralisi del nervo facciale e alterazioni atrofiche del nervo ottico (che portano a problemi oftalmologici);
- la diffusione del processo infiammatorio ai tessuti della sottocorteccia e degli emisferi cerebrali - meningoencefalite criptococcica;
- sviluppo di ascesso cerebrale (criptococcoma);
- versamento nello spazio subdurale (sotto la dura madre del cervello);
- lesione del midollo spinale;
- cambiamenti mentali e diminuzione delle funzioni cognitive.
Diagnostica meningite criptococcica
Oltre all'anamnesi e all'esame fisico, la diagnosi di infezione da C. neoformans nella meningite include necessariamente esami del sangue: clinici e biochimici generali, analisi del siero sanguigno per anticorpi alle proteine di C. neoformans ed emocoltura.
Viene eseguita una puntura lombare e viene effettuataun'analisi del liquido cerebrospinale per l'antigene e un'analisi batterioscopica (coltura batterica) del liquido cerebrospinale. [ 11 ]
La diagnostica strumentale viene effettuata mediante radiografia del torace e risonanza magnetica dell'encefalo.
Diagnosi differenziale
La diagnosi differenziale comprende la meningite e la meningoencefalite di eziologia batterica e virale, il danno cerebrale causato dai funghi Histoplasma capsulatum, Coccidioides immitis, Blastomyces dermatidis o amebe (inclusa Naegleria fowleri).
Trattamento meningite criptococcica
Il trattamento eziologico è finalizzato all'eradicazione dei criptococchi, per i quali si utilizzano farmaci antimicotici.
Il regime terapeutico prevede la somministrazione endovenosa (fleboclisi, tramite catetere venoso centrale o infusione peritoneale) dell'antibiotico antimicotico polienico Amfotericina B (Amphocyl) in combinazione con il farmaco antimicotico Flucitosina (5-fluorocitosina) o Fluconazolo, ad azione fungicida e fungistatica. Il dosaggio di questi farmaci viene calcolato in base al peso corporeo del paziente.
È necessario un monitoraggio costante delle condizioni del paziente, poiché l'amfotericina B ha un effetto tossico sui reni e gli effetti collaterali della flucitosina possono includere la soppressione della funzione emopoietica del midollo osseo, l'arresto respiratorio o cardiaco, lo sviluppo di lesioni cutanee sotto forma di necrolisi epidermica, ecc.
Secondo le raccomandazioni pubblicate nell'aggiornamento 2010 dell'IDSA (Infectious Diseases Society of America), il trattamento non è cambiato da dieci anni. Il trattamento antimicotico di prima linea si basa sull'induzione, sul consolidamento e sul mantenimento dei seguenti tre tipi di pazienti: [ 12 ]
Malattie legate all'HIV
- Terapia di induzione
- Amfotericina B desossicolato (0,7-1,0 mg/kg/giorno) + flucitosina (100 mg/kg/giorno per via orale) per 2 settimane (Evidenza A1)
- Amfotericina B liposomiale (3-4 mg/kg/giorno) o complesso lipidico amfotericina B (5 mg/kg/giorno; monitorare la funzionalità renale) + flucitosina (100 mg/kg/giorno) per 2 settimane (Evidenza B2)
- Amfotericina B desossicolato (da 0,7 a 1,0 mg/kg/giorno) o amfotericina B liposomiale (da 3 a 4 mg/kg/giorno) o complesso lipidico di amfotericina B (5 mg/kg/giorno, per i pazienti che non tollerano la flucitosina) per 4-6 settimane (Evidenza B2)
- Alternative alla terapia di induzione
- Amfotericina B desossicolato + fluconazolo (Evidenza B1)
- Fluconazolo + flucitosina (Evidenza B2)
- Fluconazolo (Evidenza B2)
- Itraconazolo (Evidenza C2)
- Fluconazolo (400 mg/die) per 8 settimane (Dati A1)
- Fluconazolo (200 mg/die) per 1 o più anni (Evidenza A1)
- Itraconazolo (400 mg/die) per 1 o più anni (Evidenza C1)
- Amfotericina B desossicolato (1 mg/kg/settimana) per 1 o più anni (Evidenza C1)
- Terapia di consolidamento
- Terapia di supporto
- Alternative alla terapia di mantenimento
Malattie correlate al trapianto
- Terapia di induzione
- Amfotericina B liposomiale (3-4 mg/kg/giorno) o complesso lipidico amfotericina B (5 mg/kg/giorno) + flucitosina (100 mg/kg/giorno) per 2 settimane (Evidenza B3)
- Alternative alla terapia di induzione
- Amfotericina B liposomiale (6 mg/kg/giorno) o complesso lipidico amfotericina B (5 mg/kg/giorno) per 4-6 settimane (Evidenza B3)
- Amfotericina B desossicolato (0,7 mg/kg/giorno) per 4-6 settimane (Evidenza B3)
- Fluconazolo (da 400 a 800 mg/die) per 8 settimane (Evidenza B3)
- Fluconazolo (da 200 a 400 mg/die) per 6 mesi a 1 anno (Evidenza B3)
- Terapia di consolidamento
- Terapia di supporto
Malattie non correlate all'HIV/trapianto
- Terapia di induzione
- Amfotericina B desossicolato (da 0,7 a 1,0 mg/kg/giorno) + flucitosina (100 mg/kg/giorno) per 4 o più settimane (Evidenza B2)
- Amfotericina B desossicolato (0,7–1,0 mg/kg/giorno) per 6 settimane (Evidenza B2)
- Amfotericina B liposomiale (3-4 mg/kg/giorno) o complesso lipidico amfotericina B (5 mg/kg/giorno) in combinazione con flucitosina, 4 settimane (Evidenza B3)
- Amfotericina B desossicolato (0,7 mg/kg/giorno) + flucitosina (100 mg/kg/giorno) per 2 settimane (Evidenza B2)
- Terapia di consolidamento
- Fluconazolo (da 400 a 800 mg/die) per 8 settimane (Evidenza B3)
- Fluconazolo (200 mg/die) per 6-12 mesi (Evidenza B3)
- Terapia di supporto
La combinazione di amfotericina B e flucitosina ha dimostrato di essere la più efficace nell'eliminare l'infezione e ha mostrato un maggiore beneficio in termini di sopravvivenza rispetto alla sola amfotericina. Tuttavia, a causa del suo costo, la flucitosina è spesso non disponibile in contesti con risorse limitate e con un elevato carico di malattia. Sono state studiate combinazioni di amfotericina B e fluconazolo che hanno mostrato risultati superiori rispetto alla sola amfotericina B.[ 13 ], [ 14 ], [ 15 ]
In assenza di trattamento, il decorso clinico progredisce fino a confusione, convulsioni, riduzione del livello di coscienza e coma.
La cefalea refrattaria agli analgesici può essere trattata con decompressione spinale dopo un'adeguata valutazione neuroradiologica con TC o RM. Il volume massimo sicuro di liquido cerebrospinale che può essere drenato con una singola puntura lombare non è chiaro, ma spesso vengono rimossi fino a 30 ml, controllando la pressione dopo ogni prelievo di 10 ml.[ 16 ]
Prevenzione
La prevenzione dell'infezione da Cryptococcus neoformans è necessaria, prima di tutto, nei casi di sistema immunitario debole. [ 17 ] Si raccomanda di evitare luoghi polverosi e di lavorare con il suolo, e le persone infette da HIV dovrebbero ricevere una terapia antiretrovirale continuativa.
Previsione
Senza trattamento, la prognosi per qualsiasi meningite fungina è infausta.
La prognosi iniziale dipende da fattori predittivi di mortalità come i seguenti [ 18 ], [ 19 ]:
- La pressione di apertura del liquido cerebrospinale è superiore a 25 cm H2O.
- Basso numero di globuli bianchi nel liquido cerebrospinale
- Disturbo sensoriale
- Diagnosi tardiva
- Titoli antigenici elevati nel liquido cerebrospinale
- Tasso di guarigione dell'infezione
- La quantità di lievito nel liquido cerebrospinale supera i 10 mm3 ( pratica comune in Brasile) [ 20 ]
- Pazienti non HIV-correlati e fattori prognostici in questi pazienti, oltre a quelli già menzionati:
- Marcatori di una risposta infiammatoria debole
- Nessun mal di testa
- neoplasia ematologica primaria
- Malattia renale o epatica cronica
La mortalità varia da Paese a Paese a seconda delle risorse disponibili. Rimane elevata negli Stati Uniti e in Francia, con tassi di mortalità a 10 settimane che vanno dal 15% al 26%, e ancora più elevati nei pazienti non infetti da HIV a causa della diagnosi tardiva e delle risposte immunitarie disfunzionali. D'altra parte, nei Paesi con risorse limitate, la mortalità aumenta dal 30% al 70% a 10 settimane a causa della presentazione tardiva e della mancanza di accesso a farmaci, misuratori della pressione arteriosa e un monitoraggio ottimale.

