Esperto medico dell'articolo
Nuove pubblicazioni
Microadenoma ipofisario: cause, sintomi, pericolo, prognosi
Ultima recensione: 12.07.2025

Tutti i contenuti di iLive sono revisionati o verificati da un punto di vista medico per garantire la massima precisione possibile.
Abbiamo linee guida rigorose in materia di sourcing e colleghiamo solo a siti di media affidabili, istituti di ricerca accademici e, ove possibile, studi rivisti dal punto di vista medico. Nota che i numeri tra parentesi ([1], [2], ecc.) Sono link cliccabili per questi studi.
Se ritieni che uno qualsiasi dei nostri contenuti sia impreciso, scaduto o comunque discutibile, selezionalo e premi Ctrl + Invio.
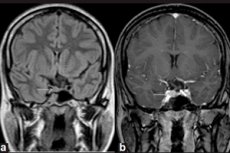
Le neoplasie benigne che si formano nelle ghiandole endocrine sono chiamate adenomi, mentre il microadenoma dell'ipofisi è un piccolo tumore del lobo anteriore della ghiandola pituitaria, che produce numerosi ormoni importanti.
Epidemiologia
L'incidenza dei tumori pituitari è stimata tra il 10 e il 23% e gli adenomi pituitari, che possono avere varie forme e dimensioni, sono i più comuni (16%).[ 1 ]
Fino al 20-25% delle persone può avere piccoli tumori pituitari, microadenomi, senza nemmeno saperlo; in circa la metà dei casi, tali tumori vengono scoperti casualmente durante un esame di diagnostica per immagini del cervello.
I microadenomi secernenti prolattina rappresentano il 45-75% di tali tumori; le formazioni che producono ACTH non superano il 14% dei casi e la frequenza dei microadenomi che producono STH non supera il 2%.
Il microadenoma dell'ipofisi nei bambini e negli adolescenti viene rilevato nel 10,7-28% dei casi e almeno la metà di essi è ormonalmente inattiva. [ 2 ]
Le cause microadenomi ipofisari
Gli esperti non conoscono le cause precise della comparsa del microadenoma nella ghiandola pituitaria, una ghiandola endocrina del cervello le cui cellule producono:
- corticotropina o ACTH – ormone adrenocorticotropo, che provoca la secrezione di ormoni steroidei da parte della corteccia surrenale;
- ormone della crescita STH – ormone somatotropico;
- gonadotropine FSH – ormone follicolo-stimolante e LH – ormone luteinizzante, che determinano la produzione degli ormoni sessuali femminili nelle ovaie e degli ormoni sessuali maschili nei testicoli;
- ormone lattogenico prolattina (PRL);
- tireotropina o ormone tireostimolante (TSH), che stimola la sintesi degli ormoni da parte della tiroide.
Si ritiene che lo sviluppo di queste neoplasie possa essere causato da traumi cranici, insufficiente apporto di sangue alla ghiandola pituitaria, infezioni cerebrali o esposizione a tossine (che causano edema e ipertensione intracranica).
Fattori di rischio
È noto che adenomi e microadenomi ipofisari si verificano più spesso in presenza di una storia familiare di sindrome MEN 1 - adenomatosi endocrina multipla di tipo 1, che è ereditaria. Esistono quindi fattori di rischio geneticamente determinati associati a determinate alterazioni del DNA. [ 3 ]
Neoplasia endocrina multipla di tipo 4 (MEN4): la MEN 4 presenta una mutazione nel gene dell'inibitore della chinasi ciclina-dipendente 1 B (CDKN1B), che è caratterizzato da tumori pituitari, iperparatiroidismo, tumori neuroendocrini dei testicoli e della cervice.[ 4 ]
Complesso di Carney (CNC): nel complesso di Carney, c'è una mutazione germinale nel gene soppressore del tumore PRKAR1A che porta alla malattia surrenalica nodulare pigmentata primaria (PPNAD), tumori testicolari, noduli tiroidei, iperpigmentazione a chiazze della pelle e acromegalia.[ 5 ]
La forma clinica degli adenomi ipofisari isolati familiari (FIPA) è caratterizzata da difetti genetici nel gene della proteina interagente con il recettore degli idrocarburi arilici (AIP), in circa il 15% di tutte le famiglie correlate e nel 50% di quelle omogenee di somatotropina.[ 6 ]
Adenomi ipofisari isolati familiari (FIPA): una mutazione nella proteina interagente con il recettore degli idrocarburi arilici (AIP) viene rilevata nell'adolescenza o nella prima età adulta in circa il 15% di tutti i casi di FIPA. Questi tumori sono tipicamente aggressivi e il più delle volte secernono l'ormone della crescita, causando acromegalia.[ 7 ]
Non si esclude la possibilità che questo tipo di tumore derivi da disturbi funzionali di altre ghiandole endocrine e strutture cerebrali, in particolare da alterazioni del sistema vascolare dell'ipotalamo, che nell'ambito del sistema neuroendocrino ipotalamo-ipofisario regola il funzionamento dell'ipofisi e del suo lobo anteriore, l'adenoipofisi, con i suoi ormoni di rilascio.
Patogenesi
L'adenoma pituitario è un tumore benigno in base all'istologia; a seconda delle dimensioni, queste neoplasie si distinguono in microadenomi (fino a 10 mm di diametro nel punto più largo), macroadenomi (10-40 mm) e adenomi giganti (40 mm o più).
Studiando la patogenesi della formazione tumorale nella ghiandola pituitaria, non è ancora stato possibile determinare i meccanismi della trasformazione iperplastica delle cellule del suo lobo anteriore in tumore.
Gli esperti ritengono che una delle versioni più convincenti sia quella legata alla deregolamentazione del metabolismo del neurotrasmettitore e ormone dopamina (che è il principale inibitore della secrezione di prolattina) e/o a un'interruzione delle funzioni dei recettori transmembrana della dopamina delle cellule pituitarie che secernono PRL (lattotrofi).
La maggior parte dei microadenomi ipofisari è sporadica, ma alcuni si verificano nell'ambito di sindromi neuroendocrine geneticamente determinate come la MEN 1, la sindrome di McCune-Albright, la sindrome di Werner e la sindrome di Carney (o complesso di Carney). Quest'ultima è associata a un aumentato rischio di sviluppare tumori benigni nelle ghiandole ormonali (endocrine), tra cui ipofisi, surrene, tiroide, ovaie e testicoli.
Sintomi microadenomi ipofisari
Un microadenoma ipofisario può non mostrare alcun sintomo per molto tempo. I sintomi variano a seconda della sede e di solito sono dovuti a una disfunzione endocrina. Questo è il riscontro più comune nei casi di squilibrio ormonale associato a un'eccessiva produzione di uno o più ormoni. Nella maggior parte dei casi, per sede, si tratta di un microadenoma dell'ipofisi anteriore.
Esistono diversi tipi di microadenoma ipofisario in base alla loro attività ormonale. Pertanto, il tipo più comune è considerato un adenoma non funzionante, ovvero un microadenoma ipofisario ormonalmente inattivo, che, finché non raggiunge una certa dimensione, non provoca alcun sintomo. Tuttavia, un microadenoma ipofisario ormonalmente inattivo in crescita può comprimere le strutture cerebrali vicine o i nervi cranici, quindi un microadenoma ipofisario e mal di testa nelle regioni frontali e temporali possono essere combinati, [ 8 ] e sono possibili anche problemi di vista. [ 9 ] Tuttavia, come affermano i ricercatori, i tumori ipofisari non funzionanti (ormonalmente inattivi) nel 96,5% dei casi sono macroadenomi. [ 10 ]
Può anche verificarsi un microadenoma ipofisario (lobo anteriore) ormonalmente attivo con aumentata secrezione dell'ormone prolattina: il prolattinoma ipofisario. L'aumentata produzione di prolattina da parte delle cellule lattotropiche dell'adenoipofisi è definita iperprolattinemia nel microadenoma ipofisario.
Come si manifesta un microadenoma ipofisario di questo tipo nelle donne? Livelli patologicamente elevati di questo ormone inibiscono la produzione di estrogeni e i primi segni si manifestano con disturbi del ciclo mestruale, con l'assenza di mestruazioni (amenorrea) e/o la loro fase ovulatoria. Di conseguenza, si sviluppa una sindrome galattorrea-amenorrea persistente e si perde la capacità di concepire e rimanere incinta.
Negli uomini, il microadenoma pituitario secernente prolattina può causare ipogonadismo iperprolattinemico con calo della libido, disfunzione erettile, ingrossamento del seno (ginecomastia) e diminuzione dei peli sul viso e sul corpo.
La microadenosi attiva secernente corticotropina (ACTH) provoca un eccesso di ormoni steroidei (glucocorticoidi) prodotti dalla corteccia surrenale, che può causare la malattia di Itsenko-Cushing di origine pituitaria.
Nei bambini, un microadenoma di questo tipo può manifestarsi con sintomi di ipercorticismo (sindrome di Cushing), tra cui mal di testa, debolezza generale, accumulo eccessivo di tessuto adiposo sul tronco, diminuzione della densità minerale ossea e della forza muscolare, atrofia della pelle a strisce (sotto forma di strie viola), ecc.
In presenza di un microadenoma attivo produttore di somatotropina, il livello di STH nell'organismo aumenta. Nell'infanzia, il suo eccessivo effetto anabolico stimola la crescita di quasi tutte le ossa del corpo e può portare al gigantismo; negli adulti, può svilupparsi acromegalia con un'eccessiva crescita delle ossa facciali (causando una distorsione dell'aspetto) e della cartilagine nelle articolazioni degli arti (che porta a una violazione delle loro proporzioni e all'ispessimento delle dita), con dolori articolari, sudorazione e secrezione sebacea eccessive e ridotta tolleranza al glucosio.
Molto raramente (nell'1-1,5% dei casi) si verifica un microadenoma della ghiandola pituitaria che produce tireotropina e poiché questo ormone ha un effetto stimolante sulla tiroide, i pazienti presentano segni clinici di ipertiroidismo pituitario sotto forma di tachicardia sinusale e fibrillazione atriale del cuore, aumento della pressione sanguigna, diminuzione del peso corporeo (con aumento dell'appetito), nonché aumentata eccitabilità nervosa e irritabilità.
Il cosiddetto microadenoma intrasellare dell'ipofisi, sinonimo di microadenoma endosellare dell'ipofisi, come l'intera ipofisi, è localizzato all'interno della sella turcica, ovvero all'interno della depressione anatomica a forma di sella nell'osso sfenoide della base cranica. Allo stesso tempo, l'ipofisi si trova sul fondo di questa depressione, nella fossa ipofisaria (regione intrasellare). La differenza sostanziale sta nel fatto che "dentro" in latino è intra, e in greco - endom.
Ma un microadenoma pituitario con crescita soprasellare significa che la neoplasia cresce verso l'alto a partire dal fondo della fossa pituitaria.
Il microadenoma cistico dell'ipofisi ha una struttura chiusa a forma di sacco ed è una formazione asintomatica.
Un microadenoma della ghiandola pituitaria con emorragia può essere il risultato di un'apoplessia o di un infarto emorragico associati all'ingrossamento della ghiandola e al danno ai capillari sinusoidali del parenchima del suo lobo anteriore, alle sinapsi neuroemali e/o ai vasi portali.
Microadenoma dell'ipofisi e gravidanza
Come già accennato, le donne con microadenoma ipofisario prolattina-secernente sono solitamente sterili a causa della carenza di estrogeni e della soppressione della secrezione pulsatile di GnRH (ormone di rilascio delle gonadotropine). Per rimanere incinta, i livelli di prolattina devono essere normalizzati, altrimenti il concepimento non avviene o la gravidanza viene interrotta all'inizio.
- È possibile partorire con un microadenoma ipofisario?
Nelle donne con microadenomi clinicamente funzionanti trattate con agonisti della dopamina (Cabergolina o Dostinex), i livelli di prolattina possono normalizzarsi e i cicli mestruali e la fertilità possono essere ripristinati.
È possibile allattare al seno se si ha un microadenoma ipofisario?
Nel periodo postpartum, l'allattamento al seno è consentito in assenza di sintomi del tumore, ma è necessario monitorarne le dimensioni (utilizzando la risonanza magnetica cerebrale). Se il tumore cresce, l'allattamento al seno viene interrotto.
- Microadenoma dell'ipofisi e fecondazione in vitro
Per la fecondazione in vitro è necessario il trattamento dell'iperprolattinemia e la procedura può essere avviata se i livelli normali di prolattina sono stabili da 12 mesi e non si riscontrano anomalie nei livelli sierici di altri ormoni pituitari.
Complicazioni e conseguenze
Quali sono i pericoli del microadenoma ipofisario? Sebbene questo tumore sia benigno, la sua presenza può causare complicazioni e avere conseguenze, in particolare:
- portare alla disfunzione del sistema ipotalamo-ipofisi-surrene con lo sviluppo della malattia di Itsenko-Cushing;
- interrompono la regolazione ormonale del ciclo mestruale nelle donne e portano alla disfunzione erettile negli uomini;
- causare ritardo della crescita e nanismo ipofisario (ipopituitarismo) nei bambini;
- provocare lo sviluppo dell'osteoporosi.
Quando un tumore in crescita comprime le fibre del nervo ottico nella zona del loro incrocio (che nell'80% delle persone si trova direttamente sopra l'ipofisi), si verifica un disturbo della mobilità oculare (oftalmoplegia) e un graduale deterioramento della visione periferica. Sebbene i microadenomi siano solitamente troppo piccoli per esercitare tale pressione.
Un microadenoma ipofisario può guarire? Non può guarire, ma nel tempo, un tumore ormonalmente inattivo nei bambini può ridursi significativamente. Tuttavia, in circa il 10% dei pazienti, i microadenomi possono aumentare di dimensioni.
Diagnostica microadenomi ipofisari
Per diagnosticare un microadenoma ipofisario sono necessari un'anamnesi completa del paziente e degli esami di laboratorio: esami del sangue per i livelli degli ormoni (prodotti dall'ipofisi), incluso un radioimmunotest del siero sanguigno per i livelli di prolattina.
Se la prolattina è normale in presenza di un microadenoma ipofisario, questo tumore è ormonalmente inattivo. Ma se sono presenti sintomi di prolattinoma, un risultato falso negativo potrebbe essere dovuto a un errore di laboratorio o allo sviluppo di un macroadenoma che comprime il peduncolo ipofisario da parte del paziente.
Inoltre, potrebbero essere necessari esami supplementari, ad esempio per il livello degli ormoni tiroidei (T3 e T4), delle immunoglobuline, dell'interleuchina-6 nel siero sanguigno.
Il microadenoma può essere rilevato solo con la diagnostica strumentale, utilizzando la risonanza magnetica (RM) dell'encefalo. La RM per il microadenoma è considerata la visualizzazione standard, con una sensibilità della RM con contrasto del 90%.
I segni di microadenoma ipofisario rilevati tramite risonanza magnetica includono: volume della ghiandola sul lato del microadenoma; aumento delle dimensioni della sella turcica; assottigliamento e modificazioni del contorno del suo fondo (parete inferiore); deviazione laterale dell'infundibolo ipofisario; isointensità dell'area arrotondata rispetto alla materia grigia nelle immagini pesate in T1 e T2; lieve iperintensità nelle immagini pesate in T2. [ 11 ]
Diagnosi differenziale
La diagnosi differenziale viene effettuata con craniofaringioma, tumore a cellule granulari (coristoma) dell'ipofisi, cisti della tasca di Rathke, formazione dermoide, infiammazione dell'ipofisi - ipofisite autoimmune o linfocitaria, feocromocitoma, malattie della tiroide, ecc.
Nelle donne con ciclo anovulatorio si distingue il microadenoma ipofisario dalla sindrome dell'ovaio policistico, poiché il 75-90% dei casi di mancata ovulazione è conseguenza della sindrome dell'ovaio policistico.
Chi contattare?
Trattamento microadenomi ipofisari
In caso di adenomi e microadenomi dell'ipofisi, il trattamento può essere medico e chirurgico. Allo stesso tempo, se i tumori sono asintomatici, si raccomanda di monitorarli, ovvero eseguire periodicamente una risonanza magnetica, per non perdere l'inizio della loro crescita.
La prescrizione di un determinato farmaco è determinata dal tipo di tumore di cui soffre il paziente.
La farmacoterapia dei tumori secernenti PRL viene effettuata con farmaci del gruppo degli stimolatori dei recettori della dopamina D2 dell'ipotalamo (agonisti selettivi della dopamina) e i più utilizzati sono Bromocriptina (Parlodel, Bromergol), Norprolac e il derivato dell'ergot Cabergolina o Dostinex per il microadenoma ipofisario con aumentata secrezione di prolattina.
Gli effetti collaterali di Dostinex (Cabergolina) possono includere reazioni allergiche; mal di testa e vertigini; nausea, vomito e dolore addominale; stitichezza; sensazione di debolezza o affaticamento; disturbi del sonno. Tra gli effetti collaterali della Bromocriptina (oltre alle reazioni allergiche) figurano dolore al petto; aumento della frequenza cardiaca e respiratoria con sensazione di mancanza di respiro; tosse con sangue; deterioramento della coordinazione dei movimenti, ecc.
I farmaci Octreotide (Sandostatin), Lanreotide (Somatuline), Pegvisomant, utilizzati per i micro- e macroadenomi che secernono l'ormone della crescita, sono inibitori dell'STH e antagonisti dei suoi recettori.
Per le neoplasie secernenti ACTH dell'adenoipofisi con sindrome di Itsenko-Cushing si utilizzano Metirapone (Metopirone) o Mitotano (Lysodren).
Il trattamento chirurgico dovrebbe essere preso in considerazione per i microadenomi funzionanti (ormonalmente attivi). Nei casi in cui il trattamento conservativo sia inefficace e il tumore presenti una lieve espansione soprasellare all'interno della sella turcica, può essere prescritta un'adenomectomia ipofisaria, un intervento chirurgico per rimuovere il microadenoma ipofisario. Attualmente, si esegue la microdissezione transnasale o transfenoidale, ovvero la rimozione del microadenoma ipofisario attraverso il naso.
Le possibili complicazioni e conseguenze della rimozione del microadenoma ipofisario includono emorragia postoperatoria e perdita di liquido cerebrospinale (che spesso richiede un reintervento), nonché infiammazione delle meningi, compromissione della vista, formazione di ematomi, diabete insipido transitorio e recidiva del microadenoma.
L'omeopatia per il microadenoma ipofisario con iperprolattinemia utilizza farmaci la cui azione può contribuire ad alleviare parzialmente i sintomi. Ad esempio, per le mestruazioni irregolari e l'amenorrea, vengono prescritti un rimedio a base di nero di seppia (Sepia) e un rimedio a base di Pulsatilla (Pulsatum pratensis), mentre per la galattorrea viene prescritto un rimedio a base di radice di ciclamino europeo.
Ovviamente, non si dovrebbe sperare che il trattamento popolare per il microadenoma ipofisario possa essere più efficace. E non solo perché con questa diagnosi gli erboristi si basano esclusivamente sui disturbi dei pazienti (senza conoscerne la vera eziologia), ma anche a causa dell'inaffidabilità di molti "rimedi popolari". Non c'è bisogno di andare lontano per trovare esempi.
Alcune fonti online consigliano di utilizzare una miscela di primula, radice di zenzero e semi di sesamo per ridurre i livelli di prolattina. Tuttavia, la primula aiuta a combattere la tosse secca prolungata e a fluidificare il catarro, mentre la radice di zenzero, come i semi di sesamo, possiede proprietà lattogeniche.
Si può anche trovare il consiglio di assumere una tintura di cimicifuga. Ma, in realtà, questo rimedio viene usato internamente per la flatulenza ed esternamente per i dolori articolari reumatici. Con ogni probabilità, la cimicifuga è stata confusa con le radici di cimicifuga nera (altri nomi sono cimicifuga nera e cimicifuga nera), che vengono utilizzate per le vampate di calore durante la menopausa.
L'alimentazione per il microadenoma ipofisario deve essere equilibrata, con un consumo ridotto di zuccheri e sale. Non si tratta di una dieta speciale, ma semplicemente di una dieta meno calorica.
In caso di microadenoma ipofisario, l'alcol è escluso.
A quale medico dovrei rivolgermi per un microadenoma ipofisario? Endocrinologi, ginecologi e neurochirurghi si occupano dei problemi che si presentano con questo tipo di tumore.
Prevenzione
Poiché le cause ambientali o legate allo stile di vita dei tumori pituitari sono sconosciute, non esiste alcun modo per prevenire lo sviluppo di microadenomi pituitari.
Previsione
La maggior parte dei tumori ipofisari è curabile. Se un microadenoma ipofisario ormonalmente attivo viene diagnosticato in tempo, le probabilità di guarigione sono elevate e la prognosi è favorevole.
Disabilità e microadenoma ipofisario: la disabilità può essere associata alla crescita tumorale e al danno al nervo ottico, nonché ad altre conseguenze di questa patologia, la cui gravità è individuale. Il riconoscimento di un paziente come disabile dipende dai problemi di salute preesistenti e dal livello di disturbi funzionali, che devono soddisfare criteri approvati dalla legge.
Microadenoma dell'ipofisi e servizio militare: i pazienti con questo tumore (anche se rimosso con successo) non devono surriscaldarsi, esporsi al sole a lungo e sottoporsi a sforzi fisici eccessivi. Pertanto, non sono adatti al servizio militare.
Quanto tempo vivono le persone con un microadenoma ipofisario? Questo tumore non è un cancro, quindi non ci sono limiti di aspettativa di vita. Tuttavia, con un microadenoma attivo secernente STH, i pazienti possono sviluppare ipertensione e un aumento delle dimensioni del cuore, il che può ridurre significativamente la loro aspettativa di vita. Un aumento del rischio di morte nei pazienti di età superiore ai 45 anni è stato osservato in caso di malattia di Itsenko-Cushing e acromegalia.

